Hvorfor har alle istopes af et element de samme kemiske peoperties?
* samme antal protoner: Isotoper af et element har det samme antal protoner, der bestemmer elementets atomnummer og dets identitet. Dette betyder, at de har det samme antal elektroner, der er ansvarlige for kemisk binding.
* forskellige antal neutroner: Isotoper adskiller sig i antallet af neutroner, de indeholder. Dette påvirker deres masse, men ikke antallet af elektroner eller protoner.
* Mindre forskelle i kemisk adfærd: Den lidt forskellige masseisotoper kan føre til meget subtile forskelle i deres kemiske reaktivitet, især i reaktioner, der involverer bindingsvibrationer eller diffusion. Disse forskelle er generelt meget små og ofte ubetydelige.
Hvorfor er forskellene så små?
* Elektroner bestemmer reaktivitet: Kemisk opførsel bestemmes primært af antallet og arrangementet af elektroner i et atom, ikke af antallet af neutroner. Da isotoper har det samme antal elektroner, har de lignende elektroniske konfigurationer og derfor lignende kemiske egenskaber.
* Masseforskelle er relativt små: Masseforskellen mellem isotoper er normalt lille sammenlignet med atomets samlede masse. Dette betyder, at forskellen i deres opførsel også er meget lille.
Eksempel:
Carbon-12 og carbon-14 er begge isotoper af kulstof. De har det samme antal protoner (6) og elektroner (6), men carbon-14 har 8 neutroner sammenlignet med carbon-12's 6 neutroner. Dette gør carbon-14 lidt tungere, men det ændrer ikke markant sin evne til at danne bindinger med andre elementer.
Kortfattet:
Mens isotoper af et element har det samme antal protoner og elektroner, adskiller de sig i antallet af neutroner. Denne forskel i masse kan føre til meget subtile variationer i deres kemiske opførsel. Til de fleste praktiske formål kan isotoper af et element imidlertid anses for at have de samme kemiske egenskaber.
Sidste artikelHvad er lipidpolymer?
Næste artikelHvor mange molekyler af ATP produceres under et kredsløb Krebs -cyklussen?
 Varme artikler
Varme artikler
-
 Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til
Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til -
 Nyt kompositmateriale har potentiale til medicinsk brugProfessor Gajanan Bhat holder et elastisk nonwoven-materiale. Kredit:Andrew Davis Tucker/UGA Forskere fra University of Georgia har udviklet et nyt materiale med egenskaber, der er ideelle til med
Nyt kompositmateriale har potentiale til medicinsk brugProfessor Gajanan Bhat holder et elastisk nonwoven-materiale. Kredit:Andrew Davis Tucker/UGA Forskere fra University of Georgia har udviklet et nyt materiale med egenskaber, der er ideelle til med -
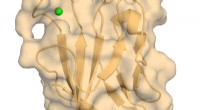 Forskere billede atomstruktur af vigtig immunregulatorHuman TIM-3 med bundet calcium. Kredit:Richard Blumberg, Brigham and Womens Hospital En ny undersøgelse foretaget af efterforskere fra Brigham and Womens Hospital giver en biofysisk og strukturel
Forskere billede atomstruktur af vigtig immunregulatorHuman TIM-3 med bundet calcium. Kredit:Richard Blumberg, Brigham and Womens Hospital En ny undersøgelse foretaget af efterforskere fra Brigham and Womens Hospital giver en biofysisk og strukturel -
 Samling af kræfterne fra elektrokemi og flowteknologiYiran Cao. Kredit:Eindhoven University of Technology Kombinationen af elektrokemi og flowteknologi lover meget for bæredygtig produktion af værdifulde kemikalier, såsom biobaserede råvarer. Fors
Samling af kræfterne fra elektrokemi og flowteknologiYiran Cao. Kredit:Eindhoven University of Technology Kombinationen af elektrokemi og flowteknologi lover meget for bæredygtig produktion af værdifulde kemikalier, såsom biobaserede råvarer. Fors
- Eksperimenter viser, at registreringen af det tidlige liv kan være fuld "falske positiver"
- Hvad er ansvarlig for absorptionen af ultraviolet stråling fra solen?
- Bio-inspireret hydrogel kan hurtigt skifte til stiv plast
- Forstå hvordan monomersekvens påvirker konduktans i molekylære ledninger
- Opdagelser på kanten af det periodiske system:Første målinger nogensinde af einsteinium
- Rapporten undersøger statens indsats for at adressere krydsfeltet mellem klimapolitik og lighedsmå…


