To atomer er isotoper af det samme element. Hvad skal der være for disse to atomer?
Samme:
* atomnummer (antal protoner): Isotoper af det samme element har det samme antal protoner. Dette definerer elementet.
* Kemiske egenskaber: Isotoper af det samme element har generelt de samme kemiske egenskaber, fordi de har det samme antal elektroner involveret i kemisk binding.
forskellige:
* massetal (antal protoner + neutroner): Isotoper adskiller sig i antallet af neutroner, de indeholder. Dette er grunden til, at isotoper af det samme element har forskellige atommasser.
* Fysiske egenskaber: Isotoper kan have lidt forskellige fysiske egenskaber, såsom smeltepunkt, kogepunkt og densitet.
Eksempel:
Carbon-12 og carbon-14 er begge isotoper af kulstof. De har det samme antal protoner (6), men carbon-14 har 8 neutroner, mens carbon-12 har 6 neutroner.
Sidste artikelHvad hedder ionisk sammensætning K2S2O3?
Næste artikelHvilke intermolekylære kræfter er til stede mellem molekyler af IF5?
 Varme artikler
Varme artikler
-
 Ny optimeringstilgang hjælper med at designe lettere kulfiberkompositmaterialerForskere fra Tokyo University of Science anvender en designtilgang til kulfibre, der optimerer fiberorientering og tykkelse for at forbedre styrken af fiberforstærket plastik, producerer lettere pla
Ny optimeringstilgang hjælper med at designe lettere kulfiberkompositmaterialerForskere fra Tokyo University of Science anvender en designtilgang til kulfibre, der optimerer fiberorientering og tykkelse for at forbedre styrken af fiberforstærket plastik, producerer lettere pla -
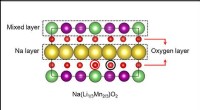 Nyt materiale kan hjælpe med at reducere batteriomkostningerne til elbiler, mobiltelefonerForskere ved University of Texas i Dallas og Seoul National University har designet et nyt batterikatodemateriale, der muligvis giver lavere omkostninger, mere miljøvenlig mulighed for lithium-ion-bat
Nyt materiale kan hjælpe med at reducere batteriomkostningerne til elbiler, mobiltelefonerForskere ved University of Texas i Dallas og Seoul National University har designet et nyt batterikatodemateriale, der muligvis giver lavere omkostninger, mere miljøvenlig mulighed for lithium-ion-bat -
 Forskere forklarer den unikke underliggende atomare struktur af PNCP metallisk glasKredit:Kumamoto University Pd42.5 Ni7,5 Cu30 P20 (PNCP) anses for at være mester for bulk metalliske glas på grund af dets glasdannende evne (GFA), men de atomare konfigurationer, der fører til den
Forskere forklarer den unikke underliggende atomare struktur af PNCP metallisk glasKredit:Kumamoto University Pd42.5 Ni7,5 Cu30 P20 (PNCP) anses for at være mester for bulk metalliske glas på grund af dets glasdannende evne (GFA), men de atomare konfigurationer, der fører til den -
 Computermodel kan hjælpe forskere med at skille sig op, gensamle proteiner på kommandoKredit:CC0 Public Domain At skilles og finde sammen igen er altid svært at gøre, men for proteiner, det er næsten umuligt. Imidlertid, en computerstyret algoritme kan hjælpe videnskabsmænd med at
Computermodel kan hjælpe forskere med at skille sig op, gensamle proteiner på kommandoKredit:CC0 Public Domain At skilles og finde sammen igen er altid svært at gøre, men for proteiner, det er næsten umuligt. Imidlertid, en computerstyret algoritme kan hjælpe videnskabsmænd med at
- Planteliv i barskoven
- Hvorfor er der farveændring i reaktionen mellem oxalsyre og kaliumpermanganat?
- En dråbe sprit og kontorlaminator giver et løft af fremstillingsevnen for nanomaterialer
- Kina suspenderer samkørsel efter mord
- Hvilke tre sydamerikanske lande passerer ækvator gennem?
- Lidt mindre kraft:At få atomkraftmikroskopi til at fungere for celler


