Hvad er forbindelser, der indeholder i bor?
uorganiske borforbindelser:
* bor trihalider: Disse inkluderer bortrifluorid (BF₃), bortrichlorid (BCL₃) og bortribromid (BBR₃). De er meget reaktive og bruges som Lewis -syrer i forskellige kemiske reaktioner.
* Boroxider: Bor danner to vigtige oxider, bortrioxid (B₂O₃) og Boron Suboxide (B₆O). Dette er vigtige komponenter i keramik, glas og andre materialer.
* bor nitrider: Boronnitrid (BN) findes i forskellige former, herunder hexagonal bornitrid (svarende til grafit) og kubisk bornitrid (svarende til diamant). De bruges i applikationer med høj temperatur og som smøremiddeladditiver.
* Borhydrider (boraner): Disse forbindelser indeholder bor- og brintatomer. Di-Borane (B₂H₆) er den enkleste boran og en nøgleforløber for andre boraner. Boraner udviser unikke bindingsstrukturer og har anvendelser i katalyse og raketbrændstoffer.
* Borates: Dette er salte eller estere af borsyre (H₃BO₃). De findes naturligt i mineraler og har anvendelser i vaskemidler, gødning og brandhæmmere.
* Borax: Dette er et naturligt forekommende bormineral, natriumtetraborat decahydrat (na₂b₄o₇ · 10H₂O). Det bruges ofte i vaskeri, rengøringsmidler og som vandblødgøringsmiddel.
organiske borforbindelser:
* organoboranes: Disse forbindelser indeholder en kulstofboronbinding. De er alsidige reagenser i organisk syntese, især til hydroborationsreaktioner.
* Borholdige polymerer: Bor kan indarbejdes i forskellige polymerer, hvilket giver egenskaber som brandhæmning, forbedret termisk stabilitet og forbedret mekanisk styrke.
* Bor-indeholdende farmaceutiske stoffer: Visse borholdige forbindelser bruges i lægemiddeludvikling, især til behandling af kræft og andre sygdomme.
Andre borholdige materialer:
* Borkarbid (B₄C): Dette er et meget hårdt og slidbestandigt keramisk materiale, der bruges i rustningsbelægning, slibende værktøjer og atomreaktorer.
* bor-dopet silicium: Bor er et almindeligt dopingmiddel i silicium til produktion af P-type halvledere, der bruges i transistorer og integrerede kredsløb.
Denne liste er på ingen måde udtømmende. Bor danner en bred vifte af forbindelser med adskillige anvendelser inden for kemi, materialevidenskab og forskellige industrier.
Sidste artikelHvad er de kemiske egenskaber ved akrilisk?
Næste artikelHvorfor er ethansyre mere farligt end saltsyre?
 Varme artikler
Varme artikler
-
 Selvhelende katalysatorfilm til brintproduktionForskning i retning af en mere effektiv brintproduktion:Stefan Barwe og hans kolleger. Kredit:RUB, Kramer Kemikere ved Center for Elektrokemiske Videnskaber ved Ruhr-Universität Bochum har udvikle
Selvhelende katalysatorfilm til brintproduktionForskning i retning af en mere effektiv brintproduktion:Stefan Barwe og hans kolleger. Kredit:RUB, Kramer Kemikere ved Center for Elektrokemiske Videnskaber ved Ruhr-Universität Bochum har udvikle -
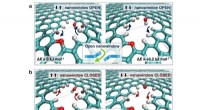 Nye mekanismer fundet til at adskille luftmolekylerFunktionel gruppeflappemekanisme i et lille nanowindow, som kan være i åben eller lukket status for at tillade O2 -gennemtrængning. Kredit:2018, Naturkommunikation , Licenseret under CC BY 4.0 N
Nye mekanismer fundet til at adskille luftmolekylerFunktionel gruppeflappemekanisme i et lille nanowindow, som kan være i åben eller lukket status for at tillade O2 -gennemtrængning. Kredit:2018, Naturkommunikation , Licenseret under CC BY 4.0 N -
 Gør det nemmere at opfange kuldioxid i cementindustrienCement er et af verdens mest almindelige byggematerialer, og dens fremstilling tegner sig for syv procent af vores drivhusgasudledning. Det er vi nødt til at gøre noget ved. Dette billede er taget i S
Gør det nemmere at opfange kuldioxid i cementindustrienCement er et af verdens mest almindelige byggematerialer, og dens fremstilling tegner sig for syv procent af vores drivhusgasudledning. Det er vi nødt til at gøre noget ved. Dette billede er taget i S -
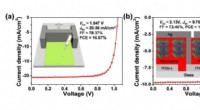 Organiske småmolekyle hultransporterende lag mod effektive p-i-n perovskit solcellerPero-SCer baseret på bladbelagt BDT-TPA-sTh HTL- og MAPbI3-aktivt lag:(a) J-V-kurver i omvendt scanningsretning; indsats:skematisk illustration af bladbelagte HTLer. (b) J-V-kurver for et 1 cm2 pero-S
Organiske småmolekyle hultransporterende lag mod effektive p-i-n perovskit solcellerPero-SCer baseret på bladbelagt BDT-TPA-sTh HTL- og MAPbI3-aktivt lag:(a) J-V-kurver i omvendt scanningsretning; indsats:skematisk illustration af bladbelagte HTLer. (b) J-V-kurver for et 1 cm2 pero-S
- Forskere udvikler en første-principper kvante Monte Carlo-pakke kaldet TurboRVB
- Hvordan genetisk baggrund former individuelle forskelle inden for en art
- Hvorfor er studiet af histologi vigtigt i din overordnede forståelse af anatomi og fysiologi?
- Sådan blandes calciumchlorid og vand
- Hvordan er teflon relateret til friktion?
- Håbets stråle? Et sted, hvor revmanta-rokker trives


