Hvorfor er ethansyre mere farligt end saltsyre?
* stærkere syre: HCI er en stærk syre, hvilket betyder, at den fuldt ud ioniserer i opløsningen og frigiver en høj koncentration af brintioner (H+). Ethansyre er en svag syre, hvilket betyder, at den kun delvist ioniserer, hvilket resulterer i en lavere koncentration af H+ -ioner. Denne forskel i surhed gør HCI mere ætsende og reaktiv.
* Korrosivitet: HCL er meget ætsende og kan forårsage alvorlige forbrændinger i hud, øjne og indre organer ved kontakt. Ethansyre er også ætsende, men dens virkninger er typisk mindre alvorlige.
* toksicitet: Mens begge syrer kan være giftige, hvis de indtages, er HCL farligere på grund af dens stærkere sure natur og potentiale til at forårsage indre forbrændinger og organskade.
* dampfarer: Røgene fra HCL er meget irriterende for respirationssystemet og kan forårsage luftvejsproblemer. Ethansyre -dampe er også irriterende, men sværhedsgraden er generelt lavere.
Der er dog nogle situationer, hvor ethansyre kan betragtes som mere farligt:
* Flammbarhed: Ethansyre er brandfarlig, mens HCL ikke er det. Dette gør ethansyre til en potentiel brandfare.
* Specifikke applikationer: I specifikke anvendelser kan egenskaberne ved ethansyre, såsom dens evne til at danne estere, udgøre en større risiko end HCL afhængigt af konteksten.
Generelt er det vigtigt at håndtere begge syrer med omhu, da de begge er farlige kemikalier. Generelt betragtes saltsyre generelt imidlertid som farligere på grund af dens stærkere surhed, højere korrosivitet og større toksicitet.
 Varme artikler
Varme artikler
-
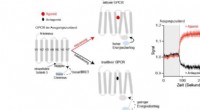 Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker
Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker -
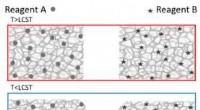 Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui
Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui -
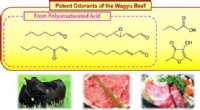 Nøgle lugtstoffer i verdens dyreste oksekød kunne hjælpe med at forklare dens tiltrækningKredit:American Chemical Society Kendt for sin bløde tekstur og karakteristiske smag, Wagyu-oksekød - ofte omtalt som Kobe-oksekød i USA - er blevet et af verdens mest eftertragtede kød. Nu i en u
Nøgle lugtstoffer i verdens dyreste oksekød kunne hjælpe med at forklare dens tiltrækningKredit:American Chemical Society Kendt for sin bløde tekstur og karakteristiske smag, Wagyu-oksekød - ofte omtalt som Kobe-oksekød i USA - er blevet et af verdens mest eftertragtede kød. Nu i en u -
 Forskere udvikler en ikke-invasiv test for røgforurening i vinmarkerKredit:CC0 Public Domain Forskere fra universiteterne i Melbourne og Adelaide har afprøvet en ikke-invasiv model til påvisning af røgforurening i vinstokke, hjælpe landmænd med at sikre kvalitetsp
Forskere udvikler en ikke-invasiv test for røgforurening i vinmarkerKredit:CC0 Public Domain Forskere fra universiteterne i Melbourne og Adelaide har afprøvet en ikke-invasiv model til påvisning af røgforurening i vinstokke, hjælpe landmænd med at sikre kvalitetsp
- Hvad er en smal passage gennem land kaldet?
- Kina månesonde kaster lys på månens mørke side
- Astrofysikere knækker sagen om forsvindende svovl i planetariske tåger
- Kemisk billeddannelse bruges til at hjælpe med diagnosticering af tyktarmskræft
- Hvor tager NASA -rumskibe af?
- Hvordan protektionisme kan hjælpe udviklingslande med at frigøre deres økonomiske potentiale


