Reagerer siliciumdioxid med HCL?
Her er hvorfor:
* siliciumdioxid er meget stabil og ureaktiv. Det har en meget stærk silicium-iltbinding, hvilket gør den modstandsdygtig over for de fleste syrer.
* Hydrochlorsyre er en svag syre. Selvom det kan reagere med nogle metaloxider, er det ikke stærkt nok til at bryde bindingerne i siliciumdioxid.
Der er nogle betingelser, hvor en reaktion kan forekomme:
* Høj temperatur: Ved meget høje temperaturer (over 800 ° C) kan siliciumdioxid reagere med HCI for at danne siliciumtetrachlorid (SICL4) og vand:
SiO2 (S) + 4HCI (G) → SICL4 (G) + 2H2O (G)
* tilstedeværelse af et stærkt oxidationsmiddel: I nærvær af stærke oxidationsmidler, såsom salpetersyre (HNO3), kan siliciumdioxid reagere med HCI for at danne siliciumtetrachlorid og vand.
Kortfattet: Under normale tilstande reagerer siliciumdioxid og saltsyre ikke.
Sidste artikelHvorfor elementer nedbrydes kemisk?
Næste artikelHvad er den kemiske reaktion for cellulær respiration?
 Varme artikler
Varme artikler
-
 Printede perovskite LED'erGrafisk repræsentation af udskrivningsprocessen for perovskite LED. Kredit:Claudia Rothkirch/HU Berlin Mikroelektronik anvender forskellige funktionelle materialer, hvis egenskaber gør dem velegne
Printede perovskite LED'erGrafisk repræsentation af udskrivningsprocessen for perovskite LED. Kredit:Claudia Rothkirch/HU Berlin Mikroelektronik anvender forskellige funktionelle materialer, hvis egenskaber gør dem velegne -
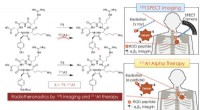 Radioisotoppar til tumordiagnose og terapiKonceptet radiotheranostics ved hjælp af At-211 og I-123 til kræftdiagnose og terapi. Kombination af SPECT-billeddannelse ved hjælp af I-123-mærket RGD-peptid med målrettet alfa-terapi ved hjælp af At
Radioisotoppar til tumordiagnose og terapiKonceptet radiotheranostics ved hjælp af At-211 og I-123 til kræftdiagnose og terapi. Kombination af SPECT-billeddannelse ved hjælp af I-123-mærket RGD-peptid med målrettet alfa-terapi ved hjælp af At -
 Dannelse af cellemembrankomponentdomæner i kunstige lipid -dobbeltlagAtomkraftmikroskopbillede af cellemembrankomponentens domæner i en flad kunstig lipid dobbeltlagsmembran. Kredit:(C) Toyohashi University of Technology. Forskning udført af Toyohashi University of
Dannelse af cellemembrankomponentdomæner i kunstige lipid -dobbeltlagAtomkraftmikroskopbillede af cellemembrankomponentens domæner i en flad kunstig lipid dobbeltlagsmembran. Kredit:(C) Toyohashi University of Technology. Forskning udført af Toyohashi University of -
 Forskere undersøgte fremstillingen af polymerfibre til brug i avanceret sundhedsplejeMohan Edirisinghe leder et team på University College London, der studerer fremstillingen af polymere nanofibre og mikrofibre - meget tynde fibre, der består af polymerer. Fibrene kan væves ind i te
Forskere undersøgte fremstillingen af polymerfibre til brug i avanceret sundhedsplejeMohan Edirisinghe leder et team på University College London, der studerer fremstillingen af polymere nanofibre og mikrofibre - meget tynde fibre, der består af polymerer. Fibrene kan væves ind i te


