Hvilke af disse forbindelser har sandsynligvis ikke ioniske bindinger LIF CH4 NAC1 eller MGF2?
* ioniske bindinger form mellem et metal og en ikke -metal. Metallet mister elektroner for at blive en positivt ladet kation, og de ikke -metale får elektroner til at blive en negativt ladet anion. De modsatte afgifter tiltrækker og danner obligationen.
Lad os analysere hver forbindelse:
* LIF (lithiumfluorid): Lithium (Li) er et metal, og fluor (F) er en ikke -metal. Dette er en klassisk ionisk binding.
* NaCl (natriumchlorid): Natrium (NA) er et metal, og chlor (CL) er en ikke -metal. Dette er også en klassisk ionisk binding.
* mgf2 (magnesiumfluorid): Magnesium (Mg) er et metal, og fluor (F) er en ikke -metal. Dette danner en ionisk binding.
* CH4 (metan): Carbon (C) og brint (H) er begge ikke -metaller. De deler elektroner i en kovalent binding , ikke en ionisk binding.
Kortfattet: Ioniske bindinger forekommer typisk mellem metaller og ikke -metaller. CH4, med to ikke -metaller, danner en kovalent binding.
 Varme artikler
Varme artikler
-
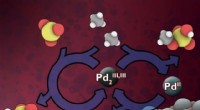 En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne
En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne -
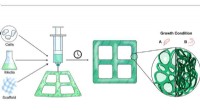 Mod tilpasset træ, dyrket i et laboratoriumI et forsøg på at levere et miljøvenligt alternativ med lavt affald, har forskere ved MIT været banebrydende med en tunbar teknik til at generere trælignende plantemateriale i et laboratorium. Kredit:
Mod tilpasset træ, dyrket i et laboratoriumI et forsøg på at levere et miljøvenligt alternativ med lavt affald, har forskere ved MIT været banebrydende med en tunbar teknik til at generere trælignende plantemateriale i et laboratorium. Kredit: -
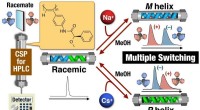 Multi-state omskiftelig stationær fase åbner nye døre i kiral adskillelseSkematisk illustration af tre-tilstands omskiftelig kiral stationær fase baseret på makromolekylær helicitetsmodulering i et poly (phenylacetylen) derivat ved hjælp af metalkationer i søjlen. Kredit:K
Multi-state omskiftelig stationær fase åbner nye døre i kiral adskillelseSkematisk illustration af tre-tilstands omskiftelig kiral stationær fase baseret på makromolekylær helicitetsmodulering i et poly (phenylacetylen) derivat ved hjælp af metalkationer i søjlen. Kredit:K -
 Team skaber bedre fingeraftryk for at opdage undvigende, værdifulde kemiske forbindelserBálint Sztáray, venstre, fra University of the Pacific, og Sandia National Laboratories kemiker David Osborn viser PEPICO-instrumentet. Kredit:Sandia National Laboratories Forestil dig at kunne se
Team skaber bedre fingeraftryk for at opdage undvigende, værdifulde kemiske forbindelserBálint Sztáray, venstre, fra University of the Pacific, og Sandia National Laboratories kemiker David Osborn viser PEPICO-instrumentet. Kredit:Sandia National Laboratories Forestil dig at kunne se
- Billeder fra International Space Station sporer fugletræk
- Estimering af dødstidspunktet under vand
- Afslører årsagen bag jetdannelse på spidsen af laseroptisk fiber
- Organiske metalramme nanoplader, der anvendes som ionbærere til selvoptimerede zinkanoder
- Hvad er hypertonisk opløsning?
- Er en tåge, hvor stjerne fødes?


