Hvad er Bohr-Rutherford-diagrammet for siliciumatom?
1. Forståelse af det grundlæggende
* Protoner og neutroner: Atomets kerne indeholder protoner (positivt ladet) og neutroner (ingen afgift).
* Elektroner: Negativt ladede elektroner kredserer kernen i energiniveauet kaldet skaller.
* atomnummer: Antallet af protoner i et atom definerer dets atomnummer. Silicons atomnummer er 14.
* Massenummer: Massenummeret er summen af protoner og neutroner. Silicon's massetal er typisk 28 (skønt der er isotoper).
2. Tegning af diagrammet
* kerne: Tegn en stor cirkel i midten for at repræsentere kernen.
* Inde i kernen skal du skrive antallet af protoner (14) og neutroner (14, siden 28 - 14 =14).
* Elektronskaller: Tegn koncentriske cirkler omkring kernen for at repræsentere elektronskaller.
* shell 1 (k shell): Denne skal kan indeholde maksimalt 2 elektroner. Tegn to elektroner som små prikker eller cirkler omkring den første cirkel.
* shell 2 (l shell): Denne skal kan indeholde maksimalt 8 elektroner. Tegn otte elektroner rundt om den anden cirkel.
* shell 3 (m shell): Denne skal kan indeholde maksimalt 18 elektroner. Tegn fire elektroner omkring den tredje cirkel. (Silicon har kun 4 elektroner i denne skal).
Her er, hvad dit Bohr-Rutherford-diagram til silicium skal se ud:
`` `
(14p, 14n)
O
/ \
/ \
O ----- o
/ \ / \
O --- o o --- o
/ \ / \
O --- o o --- o
`` `
Nøglepunkter:
* Hver elektron er repræsenteret af en lille prik eller cirkel.
* Elektronerne i hver skal skal være jævnt fordelt.
* Det er vigtigt at nøjagtigt repræsentere antallet af protoner, neutroner og elektroner i hver skal.
Vigtig note: Bohr-Rutherford-diagrammer er en forenklet model af atomet. Selvom de er nyttige til visualisering af elektronarrangement, skildrer de ikke nøjagtigt den faktiske komplekse opførsel af elektroner.
Sidste artikelHvad er et eksempel på en kemisk proces?
Næste artikelHvordan påvirker surt regnmaterialer?
 Varme artikler
Varme artikler
-
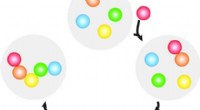 Forskere sender DNA på sekventiel byggemissionEt hold videnskabsmænd har udviklet en metode til at skabe strukturer, hvis byggesten er en milliontedel af en meter store ved at kode DNA med monteringsvejledninger. I en række eksperimenter, forsker
Forskere sender DNA på sekventiel byggemissionEt hold videnskabsmænd har udviklet en metode til at skabe strukturer, hvis byggesten er en milliontedel af en meter store ved at kode DNA med monteringsvejledninger. I en række eksperimenter, forsker -
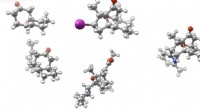 Kemikere syntetiserer psykotrope forbindelser fra regnskovstræKredit:Scripps Research Institute Barken fra Galbulimima belgraveana-træet, der kun findes i fjerntliggende regnskove i Papua Ny Guinea og det nordlige Australien, har længe været brugt af oprindel
Kemikere syntetiserer psykotrope forbindelser fra regnskovstræKredit:Scripps Research Institute Barken fra Galbulimima belgraveana-træet, der kun findes i fjerntliggende regnskove i Papua Ny Guinea og det nordlige Australien, har længe været brugt af oprindel -
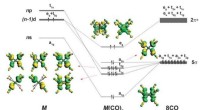 Kemikere viser, at 18-elektronprincippet ikke er begrænset til overgangsmetallerBindingsskema og form af de besatte valensorbitaler af M(CO) 8 (M =Ca, Sr, eller Ba). Opdeling af spd -valensorbitalerne i et atom M med konfigurationen (n - 1) d 2 ns 0 np 0 i oktakoordinatku
Kemikere viser, at 18-elektronprincippet ikke er begrænset til overgangsmetallerBindingsskema og form af de besatte valensorbitaler af M(CO) 8 (M =Ca, Sr, eller Ba). Opdeling af spd -valensorbitalerne i et atom M med konfigurationen (n - 1) d 2 ns 0 np 0 i oktakoordinatku -
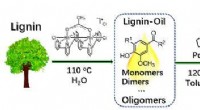 Ny strategi designet til bæredygtig produktion af benzylaminer fra ligninBæredygtig produktion af benzylaminer fra lignin. Kredit:LI Changzhi Benzylaminer, en type N-funktionaliserede aromater, anvendes i vid udstrækning som forløbere for lægemidler og syntetiske farve
Ny strategi designet til bæredygtig produktion af benzylaminer fra ligninBæredygtig produktion af benzylaminer fra lignin. Kredit:LI Changzhi Benzylaminer, en type N-funktionaliserede aromater, anvendes i vid udstrækning som forløbere for lægemidler og syntetiske farve
- Hvad er de 5 former for energi og eksempel?
- Hvordan påvirker erosion ROCK?
- Er en natriumkaliumpumpe aktiv eller passiv transport og beskriv hvorfor.?
- Project Solis hænder, ikke touchskærme, give ny mening til den digitale fremtid
- Hvad skal videnskabsmand udlede?
- Hvad passer bedst til begrebet geologisk tid et dusin år tusind hundrede eller millioner mere år?


