Hvad er den endelige temperatur af vand, hvis et metal faldt ind i det?
* Vi har brug for mere information: For at beregne den endelige temperatur har vi brug for:
* vandets oprindelige temperatur: Hvilken temperatur var vandet ved, før metallet blev tilsat?
* vandmassen: Hvor meget vand er der?
* den oprindelige temperatur på metallet: Hvilken temperatur var metallet ved, før det blev faldet i?
* Massen af metallet: Hvor meget metal er der?
* metalens specifikke varmekapacitet: Dette er en egenskab ved metallet, der fortæller os, hvor meget energi der kræves for at hæve temperaturen med et bestemt beløb. Forskellige metaller har forskellige specifikke varmekapaciteter.
Begrebet varmeoverførsel
Når det varme metal falder ned i vandet, vil varmeenergi strømmer fra det varmere metal til det køligere vand. Denne strøm fortsætter, indtil både metallet og vandet når den samme temperatur (termisk ligevægt).
Sådan beregnes den endelige temperatur
For at beregne den endelige temperatur bruger vi følgende ligning:
`` `
(Mass af vand * Specifik vandvarme * Ændring i temperaturen på vand) + (Mass af metal * Specifik metalvarme * Metalændring) =0
`` `
* Specifik vandvarme: Dette er en konstant værdi, ca. 4,184 J/g ° C.
eksempel
Lad os sige, at vi har:
* 100 g vand ved 20 ° C
* 50 g jern ved 100 ° C
* Specifik jernvarme er ca. 0,45 J/g ° C
Vi kan tilslutte disse værdier i ligningen ovenfor og løse for den endelige temperatur.
Vigtig note: Denne beregning antager, at der ikke går nogen varme til omgivelserne. I virkeligheden vil en vis varme altid gå tabt, så den endelige temperatur vil være lidt lavere end hvad der er beregnet.
Sidste artikelHvordan blev guldatomer skabt?
Næste artikelAtomer kombineres hvornår.?
 Varme artikler
Varme artikler
-
 Madrester får et dristigt nyt livKredit:University of Tokyo De fleste mennesker tænker ikke meget over de madrester, de smider; imidlertid, forskere fra Institute of Industrial Science ved University of Tokyo har udviklet en ny m
Madrester får et dristigt nyt livKredit:University of Tokyo De fleste mennesker tænker ikke meget over de madrester, de smider; imidlertid, forskere fra Institute of Industrial Science ved University of Tokyo har udviklet en ny m -
 Ingeniører bygger kemisk drevne hjul, der skifter til gear for at udføre mekanisk arbejdeAnimation fra simulering, der demonstrerer rumlig-tidsmæssig kontrol af rotorer via en kaskadereaktion. GOx-belagt rotor (magenta) ligger på venstre side af kammeret, mens CAT-belagt rotor (grøn) ligg
Ingeniører bygger kemisk drevne hjul, der skifter til gear for at udføre mekanisk arbejdeAnimation fra simulering, der demonstrerer rumlig-tidsmæssig kontrol af rotorer via en kaskadereaktion. GOx-belagt rotor (magenta) ligger på venstre side af kammeret, mens CAT-belagt rotor (grøn) ligg -
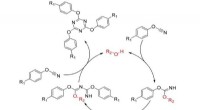 Kemikere tilbyder et nyt kig på polymerer til rumindustrienMekanisme for cyklotrimerisering af cyanatestere. Kredit:Kazan Federal University Medarbejdere ved Institut for Fysisk Kemi ved Kazan Federal University har fundet ud af, at mekanismerne til polym
Kemikere tilbyder et nyt kig på polymerer til rumindustrienMekanisme for cyklotrimerisering af cyanatestere. Kredit:Kazan Federal University Medarbejdere ved Institut for Fysisk Kemi ved Kazan Federal University har fundet ud af, at mekanismerne til polym -
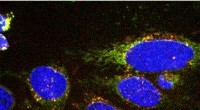 At spionere på cellers spisevaner kan hjælpe med at diagnosticere kræftForskere har udviklet en ny billedteknologi til at visualisere, hvad celler spiser, som kunne hjælpe med diagnosticering og behandling af sygdomme som kræft. Holdet har designet kemiske sonder, der ly
At spionere på cellers spisevaner kan hjælpe med at diagnosticere kræftForskere har udviklet en ny billedteknologi til at visualisere, hvad celler spiser, som kunne hjælpe med diagnosticering og behandling af sygdomme som kræft. Holdet har designet kemiske sonder, der ly
- Busser kvarts med en dråbe saltsyre?
- Atrazin ændrer kønsforholdet i Blanchards cricketfrøer
- Hvad er den omtrentlige temperatur for mesopause i en højde på 68 kilometer over havets overflade?…
- Hvad er skillnummeret for at have af planetariske systemer en galakse eller sky?
- Udslip af lattergas kan blive værre, efterhånden som klimaet opvarmes
- Hvad er miljøeffekten af sukker?


