Formaldehyd og eddikesyre har den samme empiriske formel, men forskellige?
Her er en sammenbrud:
* Empirisk formel: Det enkleste forhold mellem hele nummeret for atomer i en forbindelse. Både formaldehyd og eddikesyre har den empiriske formel ch₂o .
* molekylær formel: Det faktiske antal atomer i hvert element i et molekyle.
* formaldehyd: Ch₂o (en kulstof, to brint, et ilt)
* eddikesyre: C₂h₄o₂ (to kulstof, fire brint, to ilt)
* molekylvægt: Summen af atomvægtene for alle atomer i et molekyle.
* formaldehyd: 30 g/mol
* eddikesyre: 60 g/mol
Kortfattet:
Mens formaldehyd og eddikesyre deler den samme empiriske formel (CH₂O), adskiller de sig i deres molekylære formler og molekylvægte. Denne forskel opstår fra de forskellige arrangementer af atomer inden for deres molekyler.
 Varme artikler
Varme artikler
-
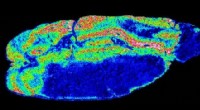 Konjugerede polymerer forbedrer massespektrometri og billeddannelseblå). Kredit:American Chemical Society Forbedringer i, hvordan prøver fremstilles, vil tilføje rækkevidde og fleksibilitet til en metode, der detekterer placeringen af udvalgte molekyler i en bi
Konjugerede polymerer forbedrer massespektrometri og billeddannelseblå). Kredit:American Chemical Society Forbedringer i, hvordan prøver fremstilles, vil tilføje rækkevidde og fleksibilitet til en metode, der detekterer placeringen af udvalgte molekyler i en bi -
 Ultrabright røntgenstråler afslører den molekylære struktur af membraner, der bruges til afsaltn…Qinyi Fu, Francisco J. Medellin-Rodriguez, Nisha Verma, og Benjamin Ocko (fra venstre mod højre) forbereder sig på at montere de membranprøver, der efterligner de membraner, der bruges i omvendt osmos
Ultrabright røntgenstråler afslører den molekylære struktur af membraner, der bruges til afsaltn…Qinyi Fu, Francisco J. Medellin-Rodriguez, Nisha Verma, og Benjamin Ocko (fra venstre mod højre) forbereder sig på at montere de membranprøver, der efterligner de membraner, der bruges i omvendt osmos -
 Forbedret katalysator kan oversætte til petrokemiske produktionsgevinsterKredit:CC0 Public Domain Aromatik er vigtige byggesten i polymerer, eller plastik, der dukker op som alt fra PET-flasker til vand til åndbare, rynkebestandigt polyestertøj. Disse petrokemikalier o
Forbedret katalysator kan oversætte til petrokemiske produktionsgevinsterKredit:CC0 Public Domain Aromatik er vigtige byggesten i polymerer, eller plastik, der dukker op som alt fra PET-flasker til vand til åndbare, rynkebestandigt polyestertøj. Disse petrokemikalier o -
 Illinois forskeres teori om pore-skala transport for at muliggøre forbedret flow batterierAdjunkt Kyle Smith. Kredit:L. Brian Stauffer. Redox-flow-batterier er en ny teknologi til elektrokemisk energilagring, der kan hjælpe med at øge brugen af strøm produceret af vedvarende energire
Illinois forskeres teori om pore-skala transport for at muliggøre forbedret flow batterierAdjunkt Kyle Smith. Kredit:L. Brian Stauffer. Redox-flow-batterier er en ny teknologi til elektrokemisk energilagring, der kan hjælpe med at øge brugen af strøm produceret af vedvarende energire


