Hvad er den afbalancerede ligning for det samlede antal gram CO2, der produceres, når 4 C tilføjes til 10,67 O2?
1. Skriv den ubalancerede ligning:
C + O₂ → CO₂
2. Balance ligningen:
C + O₂ → CO₂ (denne ligning er allerede afbalanceret)
3. Bestem den begrænsende reaktant:
* mol C: Antag, at vi har 4 gram kulstof. Den molære masse af kulstof er 12,01 g/mol.
Mol C =(4 g) / (12,01 g / mol) =0,333 mol
* mol O₂: Den molære masse af O₂ er 32,00 g/mol.
Mol O₂ =(10,67 g) / (32,00 g / mol) =0,333 mol
Da vi har lige mol af begge reaktanter, forbruges de fuldstændigt, og der er ingen begrænsende reaktant.
4. Beregn molen for co₂ produceret:
Fra den afbalancerede ligning ser vi, at 1 mol C -reagerer med 1 mol O₂ for at producere 1 mol co₂. Da vi har 0,333 mol af begge reaktanter, producerer vi 0,333 mol af co₂.
5. Beregn massen af produceret co₂:
Den molære masse af CO₂ er 44,01 g/mol.
Masse co₂ =(0,333 mol) * (44,01 g/mol) = 14,65 g
Derfor produceres 14,65 gram co₂, når 4 gram C tilsættes til 10,67 gram O₂.
Sidste artikelHvordan finder du densiteten af væske?
Næste artikelHvorfor koge væske ved et lavt tryk?
 Varme artikler
Varme artikler
-
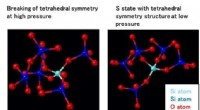 Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0
Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0 -
 Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis
Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis -
 Kobolt og wolfram - nøglen til billigere, renere brintDen nye katalysator splitter vandmolekyler for at opnå brint og oxygen med meget lave spændinger. Kredit:ICIQ Elektrolyse, spaltning af vandmolekyler med elektricitet, er den reneste måde at få br
Kobolt og wolfram - nøglen til billigere, renere brintDen nye katalysator splitter vandmolekyler for at opnå brint og oxygen med meget lave spændinger. Kredit:ICIQ Elektrolyse, spaltning af vandmolekyler med elektricitet, er den reneste måde at få br -
 Billigere brintproduktionKredit:Angewandte Chemie Elektrolytisk brintproduktion drevet af vedvarende energi ses som et miljøvenligt middel til at afhjælpe globale klima- og energiproblemer. I journalen Angewandte Chemie
Billigere brintproduktionKredit:Angewandte Chemie Elektrolytisk brintproduktion drevet af vedvarende energi ses som et miljøvenligt middel til at afhjælpe globale klima- og energiproblemer. I journalen Angewandte Chemie


