Er det en polær eller ikke -polær kovalent binding i molekyle af jod?
* Elektronegativitet: Jodatomer har den samme elektronegativitetsværdi. Elektronegativitet er et atoms evne til at tiltrække elektroner i en binding. Da de har den samme elektronegativitet, er der ingen forskel i deres evne til at tiltrække de delte elektroner.
* Lige deling: Da elektronegativitetsværdierne er identiske, deles elektronerne i bindingen lige mellem de to jodatomer. Dette resulterer i en afbalanceret fordeling af elektrondensitet.
* Intet dipolmoment: Da elektrondensiteten er jævnt fordelt, er der ingen delvis positiv eller negativ ladning på hverken jodatom. Dette betyder, at molekylet ikke har noget dipolmoment, et nøgleegenskaber for ikke -polære molekyler.
Kortfattet: Bindingen i et jodmolekyle er ikke -polært, fordi de to jodatomer har den samme elektronegativitet, hvilket fører til lige deling af elektroner og intet dipolmoment.
Sidste artikelEr oxider af gruppe 18 basic?
Næste artikelEr organiske molekyler lavet af en lille samling af enkle forløbere?
 Varme artikler
Varme artikler
-
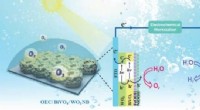 Forbedring af ydeevne til effektiv fotoelektrokemisk vandopdelingSom en af de mest lovende fotoanodekandidater til fotoelektronkemisk vandspaltning, er fotostrømtætheden og IPCE af BiVO4 blevet forbedret til 5 gange højere ved at konstruere OEC/BiVO4 og meget mat
Forbedring af ydeevne til effektiv fotoelektrokemisk vandopdelingSom en af de mest lovende fotoanodekandidater til fotoelektronkemisk vandspaltning, er fotostrømtætheden og IPCE af BiVO4 blevet forbedret til 5 gange højere ved at konstruere OEC/BiVO4 og meget mat -
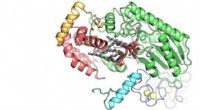 Forskere kortlægger vigtige immunsystemenzym for første gangKrystalstruktur af værtsenzymet, Acyloxyacylhydrolase (AOAH), i kompleks med lipopolysaccharid (LPS) vist med grå pinde, som er et potent bakterietoksin. Figuren viser en af de seks fedtsyrekæder af
Forskere kortlægger vigtige immunsystemenzym for første gangKrystalstruktur af værtsenzymet, Acyloxyacylhydrolase (AOAH), i kompleks med lipopolysaccharid (LPS) vist med grå pinde, som er et potent bakterietoksin. Figuren viser en af de seks fedtsyrekæder af -
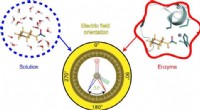 Kortlægning af elektriske felter for at hjælpe med at opklare, hvordan enzymer virkerGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00937-w Hvert øjeblik i vores krops celler forekommer utallige aktiviteter, der er livsvigtige, takket være enzymer. Disse s
Kortlægning af elektriske felter for at hjælpe med at opklare, hvordan enzymer virkerGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00937-w Hvert øjeblik i vores krops celler forekommer utallige aktiviteter, der er livsvigtige, takket være enzymer. Disse s -
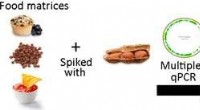 DNA-baseret metode detekterer spormængder af jordnødder i fødevarerKredit:American Chemical Society For personer med svær jordnøddeallergi, at spise selv små mængder af bælgfrugten kan udløse anafylaksi - en livstruende tilstand karakteriseret ved svimmelhed, vej
DNA-baseret metode detekterer spormængder af jordnødder i fødevarerKredit:American Chemical Society For personer med svær jordnøddeallergi, at spise selv små mængder af bælgfrugten kan udløse anafylaksi - en livstruende tilstand karakteriseret ved svimmelhed, vej


