Hvilket volumen iltgas ved 320k og 680 Torr reagerer med 2,50 L?
* Identiteten af den anden reaktant: Du skal vide, hvad iltgassen reagerer med. Dette vil bestemme støkiometrien af reaktionen.
* tryk og temperatur på den anden reaktant: For at beregne mængden af nødvendigt ilt, skal du kende betingelserne for den anden reaktant, så du kan beregne antallet af involverede mol.
Her er et eksempel på, hvordan du løser problemet, når du har disse oplysninger:
Eksempel:
Lad os sige, at iltgassen reagerer med 2,50 L brintgas ved 320 K og 680 Torr. Reaktionen er:
2 H₂ (G) + O₂ (G) → 2 H₂O (G)
1. Beregn mol brint:
* Brug den ideelle gaslov:PV =NRT
* P =680 torr =0,895 atm (konverter Torr til ATM)
* V =2,50 L
* R =0,0821 l atm/mol k
* T =320 K
* n =(pv) / (rt) =(0,895 atm * 2,50 l) / (0,0821 l atm / mol k * 320 K) =0,085 mol H₂
2. Bestem mol af iltbehov:
* Fra den afbalancerede ligning reagerer 2 mol H₂ med 1 mol O₂.
* Mol O₂ =(0,085 mol H₂) * (1 mol O₂ / 2 mol H₂) =0,0425 mol O₂
3. Beregn volumen ilt:
* Brug den ideelle gaslov igen, løs for volumen (v):
* V =(NRT) / P
* n =0,0425 mol
* R =0,0821 l atm/mol k
* T =320 K
* P =680 torr =0,895 atm
* V =(0,0425 mol * 0,0821 L ATM/Mol K * 320 K)/0,895 atm = 1,27 L O₂
Derfor ville 1,27 L iltgas ved 320 K og 680 Torr være nødvendig for at reagere med 2,50 L brintgas under de samme betingelser.
Husk: Dette er bare et eksempel. Du bliver nødt til at tilpasse beregningerne baseret på den specifikke reaktion og betingelser, der er givet i dit problem.
Sidste artikelHvilke elementer er fast væske eller gas?
Næste artikelHvordan fungerer vandmolekyler som lidt
 Varme artikler
Varme artikler
-
 Vand påvirker hyaluronans klæbrighedKredit:Ecole Polytechnique Federale de Lausanne Hyaluronsyre, også kendt som hyaluronan, er et polysaccharid, der hjælper med at fastslå viskositeten af kropsvæsker. Ifølge en ny undersøgelse af
Vand påvirker hyaluronans klæbrighedKredit:Ecole Polytechnique Federale de Lausanne Hyaluronsyre, også kendt som hyaluronan, er et polysaccharid, der hjælper med at fastslå viskositeten af kropsvæsker. Ifølge en ny undersøgelse af -
 Gennemgang af den seneste udvikling inden for elektrolyse af saltvandKredit:CC0 Public Domain Solcelledrevet teknologi, såsom fotovoltaik (PVer), kunne løse nogle af vores tids miljøudfordringer, muliggør bæredygtig produktion af elektrisk energi i mange geografisk
Gennemgang af den seneste udvikling inden for elektrolyse af saltvandKredit:CC0 Public Domain Solcelledrevet teknologi, såsom fotovoltaik (PVer), kunne løse nogle af vores tids miljøudfordringer, muliggør bæredygtig produktion af elektrisk energi i mange geografisk -
 MOF'er kan registrere og sortere besværlige gasserDenne elektrode bruges til at indsamle MOFernes sanseegenskaber. Kredit:2019 KAUST Fra astronauter og ubåde til minearbejdere og redningsarbejdere, mennesker, der opererer i små, lukkede rum har b
MOF'er kan registrere og sortere besværlige gasserDenne elektrode bruges til at indsamle MOFernes sanseegenskaber. Kredit:2019 KAUST Fra astronauter og ubåde til minearbejdere og redningsarbejdere, mennesker, der opererer i små, lukkede rum har b -
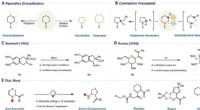 En reaktion, der fjerner svovl, nitrogen- eller oxygenatomer fra seksleddede ringe kun ved brug af b…Tilgange til piperidin-diversificering. (A) Perifer funktionalisering og skeletombygning. (B) Udvalgte eksempler på ringkontraktioner på piperidinstrukturer. (C) Grundlæggende rapport om Seebach og ko
En reaktion, der fjerner svovl, nitrogen- eller oxygenatomer fra seksleddede ringe kun ved brug af b…Tilgange til piperidin-diversificering. (A) Perifer funktionalisering og skeletombygning. (B) Udvalgte eksempler på ringkontraktioner på piperidinstrukturer. (C) Grundlæggende rapport om Seebach og ko
- Hvilket nukleotid, der driver mest energi -requy?
- Spring Heeled Jack
- Systemisk ændring af hele plastøkonomien er nødvendig for at standse havets plastikforurening
- Denne vulkan på øen Martinique dræbte næsten 30000 mennesker af en stor gassky?
- Første teoretiske bevis:Måling af et enkelt nuklear spin i biologiske prøver
- Hvilke operationer får normalt et stof til at opløses hurtigere i opløsningsmiddel, der knuser ti…


