Hvad er en biologisk virkning af hydrogenbinding mellem molekylevand?
* højt kogepunkt og smeltepunkt: Vand har et usædvanligt højt kogepunkt (100 ° C) og smeltepunkt (0 ° C) sammenlignet med andre små molekyler. Dette skyldes, at brintbindingerne kræver betydelig energi for at bryde, hvilket gør det vanskeligt at ændre Water's tilstand. Dette gør det muligt for livet at eksistere i en relativt bred temperaturområde.
* Høj varmekapacitet: Vand kan absorbere en masse varme uden at gennemgå betydelige temperaturændringer. Dette er afgørende for at opretholde stabile interne temperaturer i organismer, hvilket forhindrer hurtige ændringer, der kan være skadelige.
* Godt opløsningsmiddel: Polariteten af vandmolekyler, der er resultatet af hydrogenbinding, giver den mulighed for at opløse mange polære molekyler, som salte og sukker. Dette letter kemiske reaktioner inden for celler og transport af næringsstoffer og affaldsprodukter.
* overfladespænding: Hydrogenbinding skaber stærke sammenhængende kræfter mellem vandmolekyler, hvilket resulterer i høj overfladespænding. Dette gør det muligt for vand at danne dråber og understøtte små organismer som insekter.
* smøring: Vandets evne til at brintbinding med sig selv og andre molekyler gør det til et fremragende smøremiddel, der hjælper med bevægelse af led og væv.
Generelt er hydrogenbindingen i vand grundlæggende for livet, som vi kender det. Det bidrager til stabiliteten af celler, transport af molekyler og regulering af temperatur, hvilket gør det vigtigt for overlevelsen af alle levende organismer.
 Varme artikler
Varme artikler
-
 Nye materialer:Strålende hvid uden pigmenterEn nanostruktureret polymerfilm modelleret efter den hvide bille Cyphochilus insulanus producerer en strålende hvid belægning. Kredit:Julia Syurik, KIT Polymerfolier, der er ekstremt tynde og kend
Nye materialer:Strålende hvid uden pigmenterEn nanostruktureret polymerfilm modelleret efter den hvide bille Cyphochilus insulanus producerer en strålende hvid belægning. Kredit:Julia Syurik, KIT Polymerfolier, der er ekstremt tynde og kend -
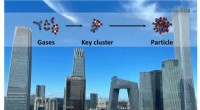 Skjulte syre-base-klynger driver hurtig dannelse af atmosfæriske ultrafine partiklerPå solrige dage i megabyer som Beijing danner gasformige syre- og baseforurenende stoffer en stor mængde nye ultrafine partikler. Klyngningen mellem en syre og en base er det hastighedsbegrænsende tri
Skjulte syre-base-klynger driver hurtig dannelse af atmosfæriske ultrafine partiklerPå solrige dage i megabyer som Beijing danner gasformige syre- og baseforurenende stoffer en stor mængde nye ultrafine partikler. Klyngningen mellem en syre og en base er det hastighedsbegrænsende tri -
 Ny teori omhandler, hvordan livet på Jorden opstod fra det oprindelige møgI begyndelsen, der var kemikalier. Kredit:Max Englund Livet på Jorden opstod i et intimt partnerskab mellem nukleinsyrerne (genetiske instruktioner for alle organismer) og små proteiner kaldet pep
Ny teori omhandler, hvordan livet på Jorden opstod fra det oprindelige møgI begyndelsen, der var kemikalier. Kredit:Max Englund Livet på Jorden opstod i et intimt partnerskab mellem nukleinsyrerne (genetiske instruktioner for alle organismer) og små proteiner kaldet pep -
 Nye molekyler afledt af cannabidiol er designet med mere potente antioxidanterImmunologi professor Eduardo Muñoz. Kredit:University of Córdoba I dag, cannabidiol er en stjernekomponent, ikke kun i kosmetikkens verden, men også inden for medicin og ernæring på grund af dets
Nye molekyler afledt af cannabidiol er designet med mere potente antioxidanterImmunologi professor Eduardo Muñoz. Kredit:University of Córdoba I dag, cannabidiol er en stjernekomponent, ikke kun i kosmetikkens verden, men også inden for medicin og ernæring på grund af dets
- Apple har design til blodtryksstyringssystem
- Hvilke virksomheder bliver børsnoteret i 2022? Næsten ingen indtil videre
- Hvor langt vil lys rejse på et halvt sekund?
- Ny computer-assisteret kemisk syntesemetode reducerer forskningstid og omkostninger
- Kompression er den del af mediet, hvor partikler er?
- Hologrammer i høj opløsning fra carbon nanorør


