Hvad er de 2 grunde til, at et fald i temperaturen bremser kemisk reaktion?
1. reduceret kollisionsfrekvens:
* Forklaring: Kemiske reaktioner forekommer, når molekyler kolliderer med tilstrækkelig energi til at bryde eksisterende bindinger og danne nye. Lavere temperaturer betyder, at molekyler har mindre kinetisk energi og bevæger sig langsommere. Dette fører til færre kollisioner pr. Tidsenhed.
* Analogi: Forestil dig et overfyldt dansegulv. Ved et langsommere tempo støder folk mindre ofte på hinanden. Tilsvarende kolliderer molekyler ved lavere temperaturer sjældnere, hvilket reducerer risikoen for reaktioner.
2. lavere aktiveringsenergibarriere:
* Forklaring: Selv hvis molekyler kolliderer, reagerer de ikke altid. Der er en energibarriere (aktiveringsenergien), som molekyler skal overvinde for at en reaktion kan forekomme. Denne energi er nødvendig for at bryde eksisterende obligationer og give nye form. Lavere temperaturer betyder, at færre molekyler har nok energi til at overgå denne barriere.
* Analogi: Forestil dig en bakke. For at komme over bakken har du brug for en bestemt mængde energi. Færre mennesker vil være i stand til at klatre op på bakken, hvis temperaturen er lav (tænk vinterforholdene), og de har mindre energi. Tilsvarende ved lavere temperaturer har færre molekyler energi til at overvinde aktiveringsenergien og reagere.
Kortfattet: Faldende temperatur påvirker både antallet af kollisioner og den tilgængelige energi til disse kollisioner, hvilket fører til en langsommere hastighed af kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Heteractis magnifica søanemoner kan hjælpe med at bekæmpe Alzheimers sygdomEn storslået søanemone, der rider på strømmen ved Madivaru Manta Point. Kredit:Neville Wootton Heteractis magnifica søanemoner indeholder neurobeskyttende peptider, der bremser inflammationsproces
Heteractis magnifica søanemoner kan hjælpe med at bekæmpe Alzheimers sygdomEn storslået søanemone, der rider på strømmen ved Madivaru Manta Point. Kredit:Neville Wootton Heteractis magnifica søanemoner indeholder neurobeskyttende peptider, der bremser inflammationsproces -
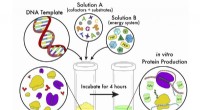 Forenklet metode gør cellefri proteinsyntese mere fleksibel og tilgængeligEn tegneserie af cellefri proteinsyntese, en bioteknologi, der udnytter cellens genetiske kode i et reagensglas. Skematikken repræsenterer en forenklet tilgang, der gør det muligt for forskere at udfø
Forenklet metode gør cellefri proteinsyntese mere fleksibel og tilgængeligEn tegneserie af cellefri proteinsyntese, en bioteknologi, der udnytter cellens genetiske kode i et reagensglas. Skematikken repræsenterer en forenklet tilgang, der gør det muligt for forskere at udfø -
 Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan
Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan -
 Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g
Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g
- Hvad er en måde at beregne massen af et objekt på, når man multiplicerer dens massefylde med hv…
- En bedre måde at bygge DNA-stilladser på
- De energimæssige implikationer af organiske radikale polymerer
- Videodommeren i søgelyset
- Invasive frøer giver invasive fugle et løft på Hawaii
- Ved at klassificere akvatiske makroinvertebrater baseret på deres bevægelse fortæller det dig om …


