Hvad opløser opløsningen af et opløst stof?
opløst: Det stof, der opløses (f.eks. Sukker, salt).
opløsningsmiddel: Det stof, der opløses (f.eks. Vand, alkohol).
Løsning: Den homogene blanding dannet, når opløsningen opløses i opløsningsmidlet.
Nøglepunkter om opløsning:
* Ingen nye kemiske bindinger dannes: Solute- og opløsningsmiddelmolekylerne forbliver intakte, bare blandet.
* Opløsningspartiklerne er omgivet af opløsningsmiddelmolekyler: Dette kaldes solvation , og det er drevet af attraktive kræfter mellem opløst stof og opløsningsmiddelmolekyler.
* Det opløste opløste stof kan ofte gendannes: For eksempel kan du fordampe vandet fra en sukkeropløsning for at få sukkeret tilbage.
Eksempler:
* sukker i vand: Sukkerkrystaller opløses i vand, bliver omgivet af vandmolekyler og danner en sukkeropløsning.
* salt i vand: Saltkrystaller opløses i vand og adskilles i natrium- og chloridioner, som er omgivet af vandmolekyler.
Faktorer, der påvirker opløsning:
* Temperatur: Generelt øger højere temperaturer hastigheden for opløsning.
* Agitation: Omrøring eller ryster hjælper med at opløse opløsningen hurtigere.
* Partikelstørrelse: Mindre opløste partikler opløses hurtigere.
* Natur af opløst stof og opløsningsmiddel: Polære opløste stoffer opløses godt i polære opløsningsmidler (f.eks. Sukker i vand), mens ikke -polære opløste stoffer opløses godt i ikke -polære opløsningsmidler (f.eks. Olie i benzin).
Kortfattet: Opløsning er en fysisk proces, hvor opløste partikler er omgivet af opløsningsmiddelmolekyler, hvilket danner en homogen blanding kaldet en opløsning. Processen er påvirket af faktorer som temperatur, agitation, partikelstørrelse og arten af opløst og opløsningsmiddel.
Sidste artikelHvad er kemi bag redox -titrering?
Næste artikelEr rent vand et stof?
 Varme artikler
Varme artikler
-
 Ny inkjet-udskrivningsmetode kunne fremskynde opdagelse af lægemidler og trykt personlig lægemidde…Tomme porer synlige i en polymerfilm, hvor dråber blev trykt, fanget og frigivet. Kredit:University of Cambridge Cambridge-ingeniører har demonstreret - for første gang - den digitale inkjet-print
Ny inkjet-udskrivningsmetode kunne fremskynde opdagelse af lægemidler og trykt personlig lægemidde…Tomme porer synlige i en polymerfilm, hvor dråber blev trykt, fanget og frigivet. Kredit:University of Cambridge Cambridge-ingeniører har demonstreret - for første gang - den digitale inkjet-print -
 Forskere skaber ny form for dyrket kødKredit:Pixabay/CC0 Public Domain McMaster-forskere har udviklet en ny form for dyrket kød ved hjælp af en metode, der lover mere naturlig smag og tekstur end andre alternativer til traditionelt kø
Forskere skaber ny form for dyrket kødKredit:Pixabay/CC0 Public Domain McMaster-forskere har udviklet en ny form for dyrket kød ved hjælp af en metode, der lover mere naturlig smag og tekstur end andre alternativer til traditionelt kø -
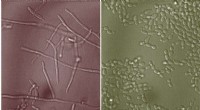 Molekyler fundet i slim kan modvirke svampeinfektionDen mere smitsomme form for gæren Candida albicans er en lang filament (til venstre). MIT-forskere har vist, at når gæren dyrkes i nærværelse af mucinglykaner, forbliver den i sin runde, harmløse form
Molekyler fundet i slim kan modvirke svampeinfektionDen mere smitsomme form for gæren Candida albicans er en lang filament (til venstre). MIT-forskere har vist, at når gæren dyrkes i nærværelse af mucinglykaner, forbliver den i sin runde, harmløse form -
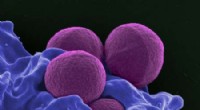 Ikke flere superbugs? Ahornsirup ekstrakt forbedrer den antibiotisk virkningEn farvet scanningselektronmikrograf af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Antibiotika redder liv hver dag, men der er en ulempe ved deres allestedsnærværende. Høje
Ikke flere superbugs? Ahornsirup ekstrakt forbedrer den antibiotisk virkningEn farvet scanningselektronmikrograf af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Antibiotika redder liv hver dag, men der er en ulempe ved deres allestedsnærværende. Høje
- Hvad ville der ske, hvis du erstattede solen med aldebaran?
- Hvorfor er Jorden så biologisk mangfoldig? Bjerge rummer svaret
- En ny tilgang til at løse fødevaresikkerhedsproblemer efter naturkatastrofer
- Hvad Nævn tre andre typer beviser for, at planter eksisterede i Antarktis.?
- Hvordan forklarer temperaturforskelle i den protoplanetære disk, der er arrangementet af planeter s…
- Hvordan kan en nebel til sidst blive et sort hul?


