Hvor mange atomer er der i 502 g Al?
1. Find den molære masse af aluminium:
* Den molære masse af aluminium er 26,98 g/mol (du kan finde dette på den periodiske tabel).
2. Beregn antallet af mol aluminium:
* Opdel massen af aluminium med dens molære masse:
* Mol Al =502 g / 26,98 g / mol =18,60 mol
3. Brug Avogadros nummer for at finde antallet af atomer:
* Avogadros nummer er 6,022 x 10^23 atomer/mol
* Multiplicer antallet af mol med Avogadros nummer:
* Antal Al -atomer =18,60 mol * 6,022 x 10^23 atomer/mol
* Antal Al -atomer =1,12 x 10^25 atomer
Derfor er der ca. 1,12 x 10^25 atomer i 502 g aluminium.
Sidste artikelHvad er udseendet af gruppe 1 -metaller?
Næste artikelHvad menes med vandfri ALCL3?
 Varme artikler
Varme artikler
-
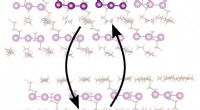 Nyt mellemprodukt opdaget til fotodissociation af triiodidanion, en klassisk lærebogsreaktionBilledet illustrerer fotodissociationen af triiodid initieret af en laserpuls og den sekundære reaktion, der fører til det nye 4-atom mellemprodukt, efterfulgt af rekombinationsreaktionen. Kredit:Bi
Nyt mellemprodukt opdaget til fotodissociation af triiodidanion, en klassisk lærebogsreaktionBilledet illustrerer fotodissociationen af triiodid initieret af en laserpuls og den sekundære reaktion, der fører til det nye 4-atom mellemprodukt, efterfulgt af rekombinationsreaktionen. Kredit:Bi -
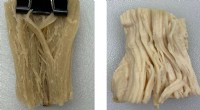 Menneskelige celler optager mindre protein fra plantebaseret kød end fra kyllingEn køderstatning (til venstre) ligner kyllingekød (til højre), men dens proteiner absorberes ikke så godt af menneskeceller. Kredit:Bearbejdet fra Journal of Agricultural and Food Chemistry 2022, DOI:
Menneskelige celler optager mindre protein fra plantebaseret kød end fra kyllingEn køderstatning (til venstre) ligner kyllingekød (til højre), men dens proteiner absorberes ikke så godt af menneskeceller. Kredit:Bearbejdet fra Journal of Agricultural and Food Chemistry 2022, DOI: -
 Ætsning af vejen til en brintøkonomi ved hjælp af plasmastrålerEt skridt tættere på en effektiv måde at producere brint på, så vi endelig kan undvære fossile brændstoffer og andre energikilder, der er skadelige for vores planet Kredit:Tokyo University of Science
Ætsning af vejen til en brintøkonomi ved hjælp af plasmastrålerEt skridt tættere på en effektiv måde at producere brint på, så vi endelig kan undvære fossile brændstoffer og andre energikilder, der er skadelige for vores planet Kredit:Tokyo University of Science -
 Ny tilgang til maskinlæring er bedre til at se enzymatiske metaller i proteinerJoanna Slusky, lektor i molekylær biovidenskab og beregningsbiologi ved University of Kansas, leder laboratoriet, hvor maskinlæring forbedrede præcisionen ved at identificere enzymatiske og ikke-enzym
Ny tilgang til maskinlæring er bedre til at se enzymatiske metaller i proteinerJoanna Slusky, lektor i molekylær biovidenskab og beregningsbiologi ved University of Kansas, leder laboratoriet, hvor maskinlæring forbedrede præcisionen ved at identificere enzymatiske og ikke-enzym
- Hvilken er ikke en stor planet i dit solsystem?
- Hvordan går frøet Absordb -vand?
- 5 månelandingsinnovationer, der ændrede livet på Jorden
- Hvorfor ændrer konstellationsposition om natten?
- Forskere og vandbehandlingsanlæg arbejder sammen om grøn vandbehandling
- Klimavenlig afkøling kan reducere år med drivhusgasemissioner og spare trillioner USD:FN


