Hvad er sandt med de fleste organiske forbindelser?
* de indeholder kulstof. Dette er det definerende kendetegn ved organiske forbindelser. Carbons evne til at danne fire obligationer giver det mulighed for at skabe lange kæder og komplekse strukturer.
* de indeholder ofte brint. Hydrogen er ofte bundet til kulstof i organiske molekyler.
* de er generelt kovalente. Organiske forbindelser holdes sammen af kovalente bindinger, hvor atomer deler elektroner.
* de er brandfarlige. Mange organiske forbindelser brænder let i nærvær af ilt.
* de har lave smelte- og kogepunkter. Sammenlignet med uorganiske forbindelser har organiske forbindelser ofte lavere smelte- og kogepunkter på grund af svagere intermolekylære kræfter.
* de er ofte uopløselige i vand. Vand er et polært opløsningsmiddel, mens mange organiske forbindelser er ikke-polære. Ligesom opløsninger som, så organiske forbindelser har en tendens til at være mere opløselige i andre organiske opløsningsmidler.
* de er forskellige i struktur og funktion. Det store antal mulige arrangementer af kulstof og andre elementer fører til en lang række organiske forbindelser med en lang række egenskaber og anvendelser.
Vigtig note: Selvom dette er almindelige egenskaber ved organiske forbindelser, er der altid undtagelser!
Sidste artikelHvor mange elektroner har en ædel gas?
Næste artikelEr organiske forbindelser lavet af sukker eller stivelse.?
 Varme artikler
Varme artikler
-
 Ikke-giftig teknologi udvinder mere guld fra malmKredit:Aalto Universitet, Robert von Bonsdorff Undersøgelse viser, at en ny chloridbaseret proces genvinder 84 % af guldet sammenlignet med de 64 %, der genvindes med traditionelle metoder. Guld
Ikke-giftig teknologi udvinder mere guld fra malmKredit:Aalto Universitet, Robert von Bonsdorff Undersøgelse viser, at en ny chloridbaseret proces genvinder 84 % af guldet sammenlignet med de 64 %, der genvindes med traditionelle metoder. Guld -
 Nyt substrat til dyb UV-overfladeforstærket resonans Raman-spredningSkematisk billede af enkeltstrenget DNA på aluminiumshullerne i et SERRS-substrat, der er bestrålet med DUV-lys. Kredit:National Tsing Hua University Den ekstreme nøjagtighed og hastighed af NBA-tr
Nyt substrat til dyb UV-overfladeforstærket resonans Raman-spredningSkematisk billede af enkeltstrenget DNA på aluminiumshullerne i et SERRS-substrat, der er bestrålet med DUV-lys. Kredit:National Tsing Hua University Den ekstreme nøjagtighed og hastighed af NBA-tr -
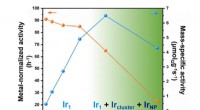 Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en
Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en -
 Bladvenestruktur kan være nøglen til at forlænge batteriets levetidNærbillede af et blad, der viser sine årer. Kredit:Christoph Rupprecht/Flickr Den naturlige struktur, der findes i blade, kan forbedre alt fra genopladelige batterier til højtydende gassensorer, i
Bladvenestruktur kan være nøglen til at forlænge batteriets levetidNærbillede af et blad, der viser sine årer. Kredit:Christoph Rupprecht/Flickr Den naturlige struktur, der findes i blade, kan forbedre alt fra genopladelige batterier til højtydende gassensorer, i
- At kaste lys over syntesen af sukkerarter før livets oprindelse
- Få to for én:Bonuselektroner i germanium nanokrystaller kan føre til bedre solceller
- Hvad observerer videnskabsmand mest?
- Nye forbindelser fra søstjerner i Kuril -bassinet viser effektivitet mod kræftceller.
- Når katastrofen rammer, NASA bringer rumets kraft
- Sådan ser du NASAs Artemis I måneraketopsendelse:TV-program, streaminginfo


