Hvordan finder du længderne af nitrogen-til-nitrogenbinding?
nitrogen-nitrogenbindinger varierer
* enkelt obligation (n-n): Den svageste type, der findes i molekyler som hydrazin (N2H4). Dette er generelt de længste N-N-obligationer.
* dobbelt obligation (n =n): Stærkere end en enkelt binding, der findes i molekyler som diazen (N2H2).
* Triple Bond (n≡n): Den stærkeste og korteste type, der findes i nitrogengas (N2).
faktorer, der påvirker bindingslængden
Bindingslængden mellem nitrogenatomer påvirkes af flere faktorer:
* obligationsordre: Når obligationsordren øges (enkelt til fordobling til tredobbelt), bliver bindingen stærkere og kortere.
* Hybridisering: Typen af hybridisering af nitrogenatomer kan påvirke bindingslængden.
* Elektrondensitet: Tilstedeværelsen af elektronoptagende eller elektron-donerende grupper i nærheden kan påvirke bindingslængden.
* stamme: I cykliske molekyler kan ringestamme påvirke bindingslængder.
hvordan man bestemmer bindingslængder
1. Eksperimentelle metoder:
* røntgenkrystallografi: Den mest nøjagtige metode tilvejebringer en 3D -struktur og præcise bindingslængder.
* Elektrondiffraktion: En anden eksperimentel teknik, der kan bestemme bindingslængder.
2. Beregningsmetoder:
* Beregninger af kvante kemi: Software som Gaussian eller ORCA kan beregne bindingslængder baseret på teoretiske modeller. Disse metoder er stadig mere nøjagtige, men kræver ekspertise.
eksempel
Lad os sige, at du vil vide N-N-bindingslængden i hydrazin (N2H4). Du kunne:
* Slå det op: Mange kemi -databaser viser bindingslængder for almindelige molekyler.
* Gør en beregning: Brug computerkemisoftware til at beregne N-N-bindingslængden i hydrazin.
Vigtig note: Data om bindingslængde er specifikke for et bestemt molekyle og dets miljø.
Sidste artikelHvad er arrangementet og bevægelsen af væske?
Næste artikelHvilken mekanisme i kroppen vil befri overskydende kemikalier?
 Varme artikler
Varme artikler
-
 Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge
Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge -
 Kemikere skaber ny diagnostisk metode til vanskelige klimaforholdKredit:CC0 Public Domain Forskere fra SCAMT Laboratory of ITMO University udviklede en metode til at påvise viralt RNA uden specielt udstyr. Sensoren er baseret på en polymerisationsreaktion:hvis
Kemikere skaber ny diagnostisk metode til vanskelige klimaforholdKredit:CC0 Public Domain Forskere fra SCAMT Laboratory of ITMO University udviklede en metode til at påvise viralt RNA uden specielt udstyr. Sensoren er baseret på en polymerisationsreaktion:hvis -
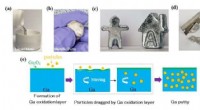 Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse
Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse -
 Ny undersøgelse ser på biologiske enzymer som kilde til brintbrændstofKemiprofessor Thomas Rauchfuss og samarbejdspartnere søger biologiske processer for at finde en effektiv kilde til brintgas som et miljøvenligt brændstof. Kredit:Fred Zwicky Forskning fra Universi
Ny undersøgelse ser på biologiske enzymer som kilde til brintbrændstofKemiprofessor Thomas Rauchfuss og samarbejdspartnere søger biologiske processer for at finde en effektiv kilde til brintgas som et miljøvenligt brændstof. Kredit:Fred Zwicky Forskning fra Universi
- Kinesiske menneskerettighedsadvokater retter blikket mod smog
- Celler produceret i slutningen af telelophase II har så mange kromosomer -celler, der startede pr…
- Hvorfor vikles ledsagerstjernen omkring Nuetron Star?
- Kan maskinlæring forbedre advarsel om debris flow?
- Sådan fungerer en gaffeltruck
- Folk i 90'erne er Australiens hurtigst voksende senioraldersgruppe


