Et metal, hvis salte er opløseligt?
Her er hvorfor:
* opløselighed er en kompleks egenskab: Opløselighed afhænger af faktorer som typen af salt, opløsningsmidlet (normalt vand), temperatur og tilstedeværelsen af andre ioner.
* De fleste metaller danner uopløselige salte: Selv meget reaktive metaller som natrium og kalium danner nogle uopløselige salte. For eksempel danner natrium et uopløseligt salt med kaliumhexanitrocobaltat (III).
* Mange metaller danner uopløselige salte med specifikke anioner: For eksempel danner de fleste metaller uopløselige salte med sulfidioner (s²⁻).
Mens der ikke er et metal med universelt opløselige salte, er nogle metaller kendt for at danne meget opløselige salte:
* gruppe 1 metaller (alkalimetaller): Disse er generelt meget reaktive, og deres salte er normalt meget opløselige.
* gruppe 2 metaller (alkaliske jordmetaller): Disse metaller har også en tendens til at danne opløselige salte med nogle undtagelser.
Husk, at der altid er undtagelser og nuancer i kemi. Hvis du har brug for at bestemme opløseligheden af et specifikt salt, skal du henvise til en opløselighedstabel eller konsultere en pålidelig kemiressource.
 Varme artikler
Varme artikler
-
 Video:Kunne der være liv uden kulstof?Kredit:The American Chemical Society Et element er rygraden i alle former for liv, vi nogensinde har opdaget på Jorden:kulstof. Nummer seks i det periodiske system er, så vidt vi ved, umuligt at
Video:Kunne der være liv uden kulstof?Kredit:The American Chemical Society Et element er rygraden i alle former for liv, vi nogensinde har opdaget på Jorden:kulstof. Nummer seks i det periodiske system er, så vidt vi ved, umuligt at -
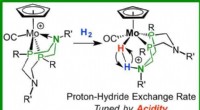 Forskere kontrollerer hastigheden af nedbrydning og fiksering af dihydrogenmolekyleDette molekyle blev genereret in situ ved hydridudvinding fra n-fluorbenzen. Kredit:Pacific Northwest National Laboratory Brint er det mest udbredte grundstof i universet. Dihydrogenmolekylet, med
Forskere kontrollerer hastigheden af nedbrydning og fiksering af dihydrogenmolekyleDette molekyle blev genereret in situ ved hydridudvinding fra n-fluorbenzen. Kredit:Pacific Northwest National Laboratory Brint er det mest udbredte grundstof i universet. Dihydrogenmolekylet, med -
 3-D-printharpikser i tandudstyr kan være giftige for reproduktiv sundhedKredit:CC0 Public Domain To kommercielt tilgængelige 3-D-printbare harpikser, som markedsføres som værende biokompatible til brug i dentale applikationer, let udvaskes forbindelser i deres omgivel
3-D-printharpikser i tandudstyr kan være giftige for reproduktiv sundhedKredit:CC0 Public Domain To kommercielt tilgængelige 3-D-printbare harpikser, som markedsføres som værende biokompatible til brug i dentale applikationer, let udvaskes forbindelser i deres omgivel -
 Ikke at tage fejl af australsk bøf – fødevareagility-projektet tackler fødevaresvindelKredit:CC0 Public Domain Tre tons australsk oksekød pakket i Casino NSW og på vej til Kina bliver sporet og verificeret ved hjælp af blockchain og Internet of Things teknologier. Forsendelsen er
Ikke at tage fejl af australsk bøf – fødevareagility-projektet tackler fødevaresvindelKredit:CC0 Public Domain Tre tons australsk oksekød pakket i Casino NSW og på vej til Kina bliver sporet og verificeret ved hjælp af blockchain og Internet of Things teknologier. Forsendelsen er
- Hvad er strøm divideret med hastighed lige?
- Sådan praktiseres beregninger for microdrops Per Minute
- Hvordan dingoer skulpturerer formen af klitter i den australske ørken
- Sådan får du flere kræftbekæmpende nanopartikler, hvor der er brug for dem
- Sådan beregnes en spændingsfald over modstande
- Opdagelsen af en ny type supernova belyser et middelalderligt mysterium


