Hvad er et volumen optaget af 0,02 mol klorgas?
1. Ideel gaslov:
Den ideelle gaslov vedrører tryk (P), volumen (V), antal mol (N) og temperatur (T):
PV =NRT
Hvor:
* R er den ideelle gaskonstant (0,0821 L · ATM/Mol · K)
2. Antagelser:
* Vi er nødt til at antage standardtemperatur og tryk (STP) for at løse dette problem. STP er defineret som 0 ° C (273,15 K) og 1 ATM -tryk.
3. Omarranger ligningen:
Løs den ideelle gaslov for volumen:
V =NRT / P
4. Tilslut værdierne:
* n =0,02 mol
* R =0,0821 l · atm/mol · k
* T =273,15 K
* P =1 atm
5. Beregn:
V =(0,02 mol * 0,0821 L · atm / mol · K * 273,15 K) / 1 atm
V ≈ 0,448 L
Derfor besættes ca. 0,448 liter volumen med 0,02 mol klorgas ved Stp.
Sidste artikelEr der en polær binding i CH4?
Næste artikelNår et bundfald dannes, er den kemiske ændring?
 Varme artikler
Varme artikler
-
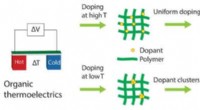 Sådan opfanges spildvarmeenergi med forbedrede polymererEt UMass Amherst-team af kemikere og elektriske ingeniører skitserer en ny måde at fremme en mere effektiv, billigere, polymer-baseret høst af varmeenergi til at producere elektricitet i et nyligt pap
Sådan opfanges spildvarmeenergi med forbedrede polymererEt UMass Amherst-team af kemikere og elektriske ingeniører skitserer en ny måde at fremme en mere effektiv, billigere, polymer-baseret høst af varmeenergi til at producere elektricitet i et nyligt pap -
 Lego-lignende kemiske byggeklodser samler sig selv til katalysator til brintbrændselscellerDen nye katalysator, en cofacial kobolt porphyrin, er skabt ved hjælp af en proces kaldet molekylær selvsamling. Under denne proces, et hætteglas fyldt med molekyler kaldet koboltporphyriner (hættegla
Lego-lignende kemiske byggeklodser samler sig selv til katalysator til brintbrændselscellerDen nye katalysator, en cofacial kobolt porphyrin, er skabt ved hjælp af en proces kaldet molekylær selvsamling. Under denne proces, et hætteglas fyldt med molekyler kaldet koboltporphyriner (hættegla -
 Millioner udsat for potentielt farlige metaller, ny teknologi kan være med til at mindske risikoenLinda Nie, en lektor ved Purdue Universitys School of Health Sciences, været med til at skabe ny teknologi for at forsøge at reducere antallet af mennesker, der er ramt af helbredsproblemer forbundet
Millioner udsat for potentielt farlige metaller, ny teknologi kan være med til at mindske risikoenLinda Nie, en lektor ved Purdue Universitys School of Health Sciences, været med til at skabe ny teknologi for at forsøge at reducere antallet af mennesker, der er ramt af helbredsproblemer forbundet -
 Stærke kunstige kulfibermuskler kan løfte 12, 600 gange deres egen vægtZoom ind på den kulfiberforstærkede oprullede muskel med en diameter på 0,4 mm. Kredit:University of Illinois Department of Mechanical Science and Engineering Optrækket, en øvelse frygtet af de fl
Stærke kunstige kulfibermuskler kan løfte 12, 600 gange deres egen vægtZoom ind på den kulfiberforstærkede oprullede muskel med en diameter på 0,4 mm. Kredit:University of Illinois Department of Mechanical Science and Engineering Optrækket, en øvelse frygtet af de fl
- Data fra NASAs Solar Dynamics Observatory giver fingerpeg om solens koronale bestråling
- Hvor langt rejser lyset fra en lommelygte?
- De molekyler, der omdanner ekstracellulære signaler til intracellulære, er?
- Hvad er definitionen af kemisk forvitring i en videnskabelig lærebog?
- Hvorfor kan vi høre andre fodspor,
- Australien er muligvis på vej mod emissionshandel mellem store forurenere


