Hvad er kemisk formel for Stannic Hypoiodite?
* "Stannic" Henviser til tin (IV) ion (SN⁴⁺), som er den højere oxidationstilstand af tin.
* "Hypoiodite" henviser til hypoioditionen (IO⁻).
Derfor er den korrekte formel for Stannic Hypoiodite SN (IO) ₄.
Forklaring:
* Det romerske tal "IV" i "Stannic" angiver, at tinionen har en +4 ladning.
* Hypoioditionen har en -1 -ladning.
* For at afbalancere ladningerne har du brug for fire hypoioditioner (4 x -1 =-4) for at neutralisere +4 ladningen af tinionen.
Vigtig note: Stannic Hypoiodite er en hypotetisk forbindelse, og der er ingen kendt bevis for, at den findes. Det er sandsynligvis ustabilt og nedbrydes let.
Sidste artikelI hvilket produkt findes natriumchlorid?
Næste artikelHvad er det mest komplekse slags organiske molekyle?
 Varme artikler
Varme artikler
-
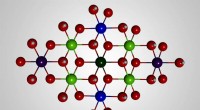 Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech-
Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech- -
 Fremskyndelse af klinisk brug af Raman-spektroskopi-kemiske fingeraftrykAfbildning af den relative andel af forskellige signalkilder i en menneskelig hjernemåling foretaget ved hjælp af et Raman-spektroskopisystem. Fra fig. 1, doi:10.1117/1.JBO.25.4.040501 Kredit:SPIE
Fremskyndelse af klinisk brug af Raman-spektroskopi-kemiske fingeraftrykAfbildning af den relative andel af forskellige signalkilder i en menneskelig hjernemåling foretaget ved hjælp af et Raman-spektroskopisystem. Fra fig. 1, doi:10.1117/1.JBO.25.4.040501 Kredit:SPIE -
 Formskiftende organiske krystaller bruger hukommelse til at forbedre plastikelektronikIllinois kemi og biomolekylær ingeniørprofessor Ying Diao, ret, og kandidatstuderende Hyunjoong Chung er en del af et team, der har identificeret en mekanisme, der udløser form-hukommelse i organiske
Formskiftende organiske krystaller bruger hukommelse til at forbedre plastikelektronikIllinois kemi og biomolekylær ingeniørprofessor Ying Diao, ret, og kandidatstuderende Hyunjoong Chung er en del af et team, der har identificeret en mekanisme, der udløser form-hukommelse i organiske -
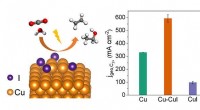 Ny katalysator øger kuldioxid elektroreduktion til multicarbon-produkterEn Cu-CuI-kompositkatalysator opnår højeffektiv produktion af C 2 + kemikalier fra elektrokatalytisk CO 2 reduktion. Kredit:LI Hefei og LIU Tianfu Elektrokatalytisk CO 2 reduktionsreaktion
Ny katalysator øger kuldioxid elektroreduktion til multicarbon-produkterEn Cu-CuI-kompositkatalysator opnår højeffektiv produktion af C 2 + kemikalier fra elektrokatalytisk CO 2 reduktion. Kredit:LI Hefei og LIU Tianfu Elektrokatalytisk CO 2 reduktionsreaktion
- NASA giver et nyt kig på Puerto Rico efter orkanen Maria
- En foldekeramik
- Undersøgelse skinner lys over alternative medicinske billeddannelsesteknikker
- Hvilken del af et atom bevæger sig, når den opkræves?
- Nye Nevada-eksperimenter har til formål at forbedre overvågningen af nukleare eksplosioner
- Monkey skruenøgle molekyle syltetøjer tuberkulose protein


