Hvad er partiklerne i flydende fast stof og gas?
solid
* Partikler er tæt pakket og arrangeret i et almindeligt, gentagende mønster (krystallinsk struktur). Dette giver faste stoffer deres konkrete form og volumen.
* Partikler vibrerer i faste positioner. De har lav kinetisk energi, hvilket betyder, at de ikke bevæger sig frit.
væske
* Partikler er tæt sammen, men kan bevæge sig rundt i hinanden. Dette giver væsker deres evne til at flyde og tage formen på deres beholder.
* Partikler har mere kinetisk energi end faste stoffer. De vibrerer og bevæger sig mere frit, men ikke så frit som gaspartikler.
gas
* Partikler er langt fra hinanden og bevæger sig tilfældigt. Dette gør gasser komprimerbare og giver dem mulighed for at udvide til at fylde enhver beholder.
* Partikler har den højeste kinetiske energi. De bevæger sig meget hurtigt og kolliderer ofte.
Vigtig note:
* Alle stofstater består af de samme grundlæggende partikler (atomer og molekyler). Det er arrangementet og bevægelsen af disse partikler, der bestemmer stoftilstanden.
* Stater af materie kan ændre sig. Tilsætning af varmeenergi øger partiklernes kinetiske energi, hvilket får dem til at bevæge sig hurtigere og overgang fra fast til væske (smelte) eller væske til gas (kogning/fordampning). Fjernelse af varmeenergi har den modsatte effekt.
Sidste artikelHvilken del af cement er kemisk?
Næste artikelKan både Rutherford og Bohrs model af Atom forklare spektre linjer elementer?
 Varme artikler
Varme artikler
-
 Forskere gør fremskridt inden for afsaltningsteknologiIllinois mekanik- og ingeniørprofessor Kyle Smith og hans medforfattere har vist, at en ny batterylignende vandafsaltningsanordning kunne hjælpe med at levere ferskvand til en række forskellige område
Forskere gør fremskridt inden for afsaltningsteknologiIllinois mekanik- og ingeniørprofessor Kyle Smith og hans medforfattere har vist, at en ny batterylignende vandafsaltningsanordning kunne hjælpe med at levere ferskvand til en række forskellige område -
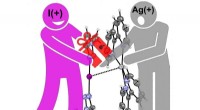 Interaktion mellem iodonium og sølvkation demonstreret for første gangSådan sker det:Positivt jod giver en elektrongave til positivt sølv. Kredit:Antonio Frontera og Kari Rissanen Et internationalt forskerhold ledet af professor Kari Rissanen fra University of Jyvas
Interaktion mellem iodonium og sølvkation demonstreret for første gangSådan sker det:Positivt jod giver en elektrongave til positivt sølv. Kredit:Antonio Frontera og Kari Rissanen Et internationalt forskerhold ledet af professor Kari Rissanen fra University of Jyvas -
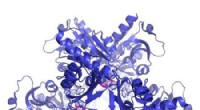 Ny tilgang gør det lettere at finde nye lægemidlerBåndrepræsentation af strukturen af et enzym kendt som ATP-PRT fra TB-bakterier (blå), bundet til en allosterisk aktivator (pink). Kredit:Luiz Carvalho Forskere har skabt en ny metode til screen
Ny tilgang gør det lettere at finde nye lægemidlerBåndrepræsentation af strukturen af et enzym kendt som ATP-PRT fra TB-bakterier (blå), bundet til en allosterisk aktivator (pink). Kredit:Luiz Carvalho Forskere har skabt en ny metode til screen -
 Enkel vandtest kunne forhindre lammende knoglesygdomDen enkle test skifter farve fra lilla til blå, når fluorindholdet er for højt. Kredit:University of Bath En enkel farveændrende test for at påvise fluor i drikkevand, udtænkt af forskere ved Univ
Enkel vandtest kunne forhindre lammende knoglesygdomDen enkle test skifter farve fra lilla til blå, når fluorindholdet er for højt. Kredit:University of Bath En enkel farveændrende test for at påvise fluor i drikkevand, udtænkt af forskere ved Univ
- Hvad er ulemperne og fordele ved chlorethen?
- Hvordan forbliver måne i kredsløb omkring solen?
- Kan kun sol- og kemiske ændringer producere lys?
- Hvad er konsolideringskoefficient?
- Hvad er den kemiske ligning for reaktioner, når kobber tilsættes til aluminiumssulfat?
- Hvilke videnskabelige principper forårsager de forskellige lag af Jorden?


