Hvorfor er formlerne af bariumchlorid og strontium ens?
* indeholder et metal fra den samme gruppe: Både barium (BA) og strontium (SR) er i gruppe 2 i den periodiske tabel, også kendt som de alkaliske jordmetaller. Dette betyder, at de begge har to valenselektroner, hvilket gør dem meget reaktive og tilbøjelige til at miste disse to elektroner til at danne en +2 ladning.
* kombineres med den samme ikke-metal: Begge forbindelser indeholder chlor (CL), et halogen i gruppe 17. Chlor har en høj elektronegativitet og har en tendens til at få et elektron til dannelse af en -1 -ladning.
Dannelse af forbindelserne:
* bariumchlorid (bacl₂): Barium (Ba²⁺) mister to elektroner til dannelse af en +2 -kation. Klor (CL⁻) får en elektron til dannelse af en -1 -anion. For at afbalancere ladningerne er der behov for to chloridioner for hver bariumion, hvilket resulterer i formlen bacl₂.
* strontiumchlorid (srcl₂): Strontium (SR²⁺) mister også to elektroner til dannelse af en +2 -kation. Igen er der behov for to chloridioner (CL⁻) for hver strontiumion for at afbalancere ladningerne, hvilket giver formlen srcl₂.
I det væsentlige stammer ligheden i deres formler fra de lignende kemiske egenskaber ved barium og strontium, begge danner +2 kationer og kombinerer med chloridioner i et forhold på 1:2.
Sidste artikelHvad er en egenskab ved forbrændingsreaktion?
Næste artikelHvordan demonstreres hydrogensulfid i Kia -medium?
 Varme artikler
Varme artikler
-
 Forskere skaber første bærbare teknologi til påvisning af cyanotoksiner i vandNorth Carolina State University forskere har udviklet den første bærbare teknologi, der kan teste for cyanotoksiner i vand. For at teste for cyanotoksiner, brugere placerer en dråbe vand på en tilpass
Forskere skaber første bærbare teknologi til påvisning af cyanotoksiner i vandNorth Carolina State University forskere har udviklet den første bærbare teknologi, der kan teste for cyanotoksiner i vand. For at teste for cyanotoksiner, brugere placerer en dråbe vand på en tilpass -
 Forskere udvikler diagnostisk værktøj til påvisning af cryptosporidiumIngeniørdoktorand George Luka siger, at der er et presserende behov for at udvikle en hurtig, fleksibel, nøjagtigt og realtidsdetektionsværktøj til at klare udfordringen med at beskytte vandforbrugere
Forskere udvikler diagnostisk værktøj til påvisning af cryptosporidiumIngeniørdoktorand George Luka siger, at der er et presserende behov for at udvikle en hurtig, fleksibel, nøjagtigt og realtidsdetektionsværktøj til at klare udfordringen med at beskytte vandforbrugere -
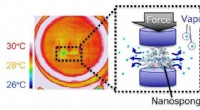 Udvikling af en ny type køling via kraftdrevet flydende gasovergangDen kølende effekt incused af sandwiched nanosvamp. Kredit:Hirotomo Nishihara Et forskerhold fra Tohoku University, Nissan Motor Co., Shinshu Universitet, og Okayama University gjorde en banebryde
Udvikling af en ny type køling via kraftdrevet flydende gasovergangDen kølende effekt incused af sandwiched nanosvamp. Kredit:Hirotomo Nishihara Et forskerhold fra Tohoku University, Nissan Motor Co., Shinshu Universitet, og Okayama University gjorde en banebryde -
 Hurtig, præcis og ikke-destruktiv:Den nye metode til at analysere fødevarekvalitetNIRS analyse af spinatplanter direkte i marken. Kredit:Universidad de Córdoba Forbrugerne leder altid efter produkter af god kvalitet, frem for alt i frisk mad som grøntsager. Men hvordan måler vi
Hurtig, præcis og ikke-destruktiv:Den nye metode til at analysere fødevarekvalitetNIRS analyse af spinatplanter direkte i marken. Kredit:Universidad de Córdoba Forbrugerne leder altid efter produkter af god kvalitet, frem for alt i frisk mad som grøntsager. Men hvordan måler vi
- Hvad hedder massenummeret minus atomik?
- Metoden afslører, hvad bakterier sanser i deres omgivelser
- Hvorfor planeterne ikke kolliderer hinanden?
- Mark Zuckerberg taler om privatlivets fred, ved et uheld disses Facebook Portal
- Et brydende teleskop producerer et billede ved hjælp af en?
- Sådan beregnes en gennemsnitsgrad


