Hvor mange atomer er der i en blanding af to elementer?
* de specifikke elementer: Forskellige elementer har forskellige atommasser, så antallet af atomer varierer.
* Massen eller molen af blandingen: Du skal kende mængden af hvert element, der er til stede i blandingen.
* om blandingen er en forbindelse eller en simpel blanding: Hvis det er en forbindelse, kan du bruge den kemiske formel til at bestemme forholdet mellem atomer.
Sådan kan du henvende dig til dette:
1. Identificer elementerne: Lad os sige, at blandingen indeholder element X og Element Y.
2. Find molmassen for hvert element: Du kan finde dette på den periodiske tabel.
3. Bestem blandingen eller molen af blandingen: Disse oplysninger er afgørende.
4. Beregn molen for hvert element: Hvis du kender blandingen af blandingen, kan du bruge masseprocentdelene for hvert element og deres molære masser til at finde mol.
5. Konverter mol til atomer: Brug Avogadros nummer (6.022 x 10^23 atomer/mol) til at konvertere mol for hvert element til antallet af atomer.
Eksempel:
Lad os sige, at du har en 10 gram blanding af kulstof (C) og ilt (O). Masseprocenten af kulstof er 25% og ilt er 75%.
1. Molmasser: Carbon (c) =12,01 g/mol, ilt (O) =16,00 g/mol.
2. masse af hvert element:
* Kulstof:10 g * 0,25 =2,5 g
* Ilt:10 g * 0,75 =7,5 g
3. mol af hvert element:
* Kulstof:2,5 g / 12,01 g / mol =0,208 mol
* Oxygen:7,5 g / 16,00 g / mol =0,469 mol
4. atomer for hvert element:
* Carbon:0,208 mol * 6,022 x 10^23 atomer/mol =1,25 x 10^23 atomer
* Oxygen:0,469 mol * 6,022 x 10^23 atomer/mol =2,82 x 10^23 atomer
Derfor ville blandingen indeholde ca. 1,25 x 10^23 carbonatomer og 2,82 x 10^23 iltatomer.
Sidste artikelHvor mange mol HCI kan 0,055 g calciumcarbonatneutralisering?
Næste artikelHvilken bindingstype er CACI2 -forbindelse?
 Varme artikler
Varme artikler
-
 Kemikere rapporterer biofornyelig, biologisk nedbrydeligt plastalternativKredit:CC0 Public Domain Colorado State University polymerkemikere har taget endnu et skridt mod en fremtid med høj ydeevne, biofornybar, biologisk nedbrydelig plast. Udgiver i Naturkommunikatio
Kemikere rapporterer biofornyelig, biologisk nedbrydeligt plastalternativKredit:CC0 Public Domain Colorado State University polymerkemikere har taget endnu et skridt mod en fremtid med høj ydeevne, biofornybar, biologisk nedbrydelig plast. Udgiver i Naturkommunikatio -
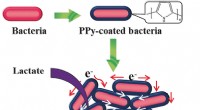 Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s -
 Neutronmicellemålinger giver indsigt i forbedret lægemiddelleveringTyler Cooksey, en kandidatforsker ved University of Houston, bruger ORNLs Bio-SANS-instrument ved High Flux Isotope Reactor til at forstå, hvordan miceller kan forbedres for at skabe mere effektive læ
Neutronmicellemålinger giver indsigt i forbedret lægemiddelleveringTyler Cooksey, en kandidatforsker ved University of Houston, bruger ORNLs Bio-SANS-instrument ved High Flux Isotope Reactor til at forstå, hvordan miceller kan forbedres for at skabe mere effektive læ -
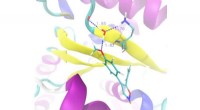 Forskere opdager nyt anti-cancer molekyleSnapshot fra simulering af molekylær dynamik af forbindelse 2c bundet til tubulin. Et system af hydrogenbindinger blev dannet, der involverer liganden, proteinresterne Asn349 og Lys352 og et vandmolek
Forskere opdager nyt anti-cancer molekyleSnapshot fra simulering af molekylær dynamik af forbindelse 2c bundet til tubulin. Et system af hydrogenbindinger blev dannet, der involverer liganden, proteinresterne Asn349 og Lys352 og et vandmolek
- Hvad er det største antal atom -enkeltbindinger et kulstof til med alle obligationer?
- Deler menneskelige embryoner og kræft den samme startsikring?
- Hvad er formålet med en videnskabelig model?
- Lunar sonic boomer
- Hvad kaldes en form for plante?
- Kvalitetsovervågning, kollegastøtte nøgle til børneværnssagsbehandlerfastholdelse


