Hvis der produceres 0,905 mol Al2O3, hvad produceres massjern også?
Her er hvorfor:
* støkiometri: Kemiske reaktioner følger loven om bevarelse af masse, hvilket betyder, at antallet af atomer i hvert element skal være det samme på begge sider af ligningen. Den afbalancerede kemiske ligning fortæller os det nøjagtige forhold mellem reaktanter og involverede produkter.
* molforhold: Den afbalancerede ligning giver os mulighed for at bestemme molforholdet mellem aluminiumoxid og jernet. Dette forhold er vigtigt for at omdanne mol af et stof til mol af et andet.
* molmasse: Når du kender molen af produceret jern, kan du bruge dens molære masse (55,845 g/mol) til at beregne jernmassen.
For at løse problemet skal du give følgende:
1. den afbalancerede kemiske ligning for reaktionen.
Eksempel:
Lad os sige, at reaktionen er:
Fe₂o₃ + 2 al → Al₂o₃ + 2 Fe
trin til at løse:
1. Balance ligningen: Ligningen er allerede afbalanceret.
2. Bestem molforholdet: Fra den afbalancerede ligning produceres 1 mol al₂o₃ for hver 2. mol Fe.
3. Beregn mol Fe: Da 0,905 mol Al₂o₃ produceres, har vi:0,905 mol al₂o₃ * (2 mol Fe / 1 mol al₂o₃) =1,81 mol Fe.
4. Beregn masse af FE: 1,81 mol Fe * (55,845 g/mol) =101 g Fe (ca.).
Derfor produceres der også 0,905 mol Al₂o₃, ca. 101 gram jern også.
Angiv den afbalancerede kemiske ligning, så vi kan løse problemet fuldstændigt.
Sidste artikelHar polære forbindelser en ujævn fordeling af elektrisk ladning?
Næste artikelHvad er atmosfærisk kemi?
 Varme artikler
Varme artikler
-
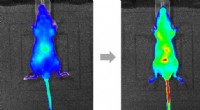 C-vitamin i kroppen kan spores ved fluorescensMusene blev injiceret med en dosis ekstra C-vitamin, hæve koncentrationen over det normale. Sondesignalet spredte sig over hele kroppen over en time, bliver særligt intens i vitale organer. Det er før
C-vitamin i kroppen kan spores ved fluorescensMusene blev injiceret med en dosis ekstra C-vitamin, hæve koncentrationen over det normale. Sondesignalet spredte sig over hele kroppen over en time, bliver særligt intens i vitale organer. Det er før -
 Trænger undervisning og kommunikation om mikrofluidiske fremskridt til forbedring?I Biomikrofluidik , forskere præsenterer en gennemgang af publiceret litteratur om mikrofluidikundervisning og giver metoder og forslag til forbedring af mikrofluidiklære og -opsøgende. Dette billed
Trænger undervisning og kommunikation om mikrofluidiske fremskridt til forbedring?I Biomikrofluidik , forskere præsenterer en gennemgang af publiceret litteratur om mikrofluidikundervisning og giver metoder og forslag til forbedring af mikrofluidiklære og -opsøgende. Dette billed -
 Sammensætning styrer biologisk ur med lysFigur:Burforbindelser regulerer det cirkadiske ur med lys (billede af Issei Takahashi, Nagoya Universitet) Forskere ved Japans Institute of Transformative Bio-Molecules (ITbM) ved Nagoya Universit
Sammensætning styrer biologisk ur med lysFigur:Burforbindelser regulerer det cirkadiske ur med lys (billede af Issei Takahashi, Nagoya Universitet) Forskere ved Japans Institute of Transformative Bio-Molecules (ITbM) ved Nagoya Universit -
 Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel
Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel
- Undersøgelse viser, hvordan et insekt fik sine vinger
- Hvad er den molekylære formel for Vineger?
- Hubble-billeder usædvanlig galakse NGC 1156
- Tilføjelse af nanopartikler til en polymermatrix forbedrer materialernes termomekaniske egenskaber
- En simpel formel, der kan være nyttig til luftrensning, rumdrift, og molekylære analyser
- Herschel og Planck udsigt over stjernedannelse


