Hvad er virkningen af at tilsætte p nitrotoluen til frysepunkt naphthalen?
Her er hvorfor:
* frysningspunktdepression: Dette er en kolligativ egenskab, hvilket betyder, at det afhænger af antallet af opløste partikler, der er til stede i en løsning, ikke deres identitet.
* opløsningsmiddel og opløsningsmiddel: I dette tilfælde er naphthalen opløsningsmidlet (det stof, der opløses det andet), og p-nitrotoluen er det opløste stof (det stof, der opløses).
* forstyrrelse af krystalgitter: Når du tilsætter P-nitrotoluen til naphthalen, forstyrrer P-nitrotoluenmolekylerne det ordnede arrangement af naphthalenmolekyler i krystalgitteret. Dette gør det sværere for naphthalenmolekylerne at danne en solid struktur.
* Nedre frysepunkt: Som et resultat er den temperatur, hvorpå naphthalenopløsningen fryser, lavere end frysningspunktet for rent naphthalen.
Nøglepunkter:
* Mængden af frysepunktdepression afhænger af koncentrationen af opløsningen (p-nitrotoluen). Jo højere koncentration, jo større er depressionen.
* Denne effekt er nyttig til bestemmelse af molekylvægten af et opløst stof (ved hjælp af en teknik kaldet kryoskopi).
Fortæl mig, hvis du gerne vil vide mere om frysepunktdepression eller andre kolligative egenskaber!
Sidste artikelSpørg os er ligningen for ethylalkohol med eddikesyre og conc. Svovlsyre?
Næste artikelDet frysende punkt for et stof er?
 Varme artikler
Varme artikler
-
 Sådan bukker du fladt glas perfekt rundt om hjørnerEt dobbeltglas hjørneelement produceret med den nye glasbukkeproces. Kredit:Fraunhofer IWM Forskere fra Fraunhofer Institute for Mechanics of Materials IWM har udviklet en ny proces, der kan bøje
Sådan bukker du fladt glas perfekt rundt om hjørnerEt dobbeltglas hjørneelement produceret med den nye glasbukkeproces. Kredit:Fraunhofer IWM Forskere fra Fraunhofer Institute for Mechanics of Materials IWM har udviklet en ny proces, der kan bøje -
 Et nyt regime til analyse af egenskaber af topologiske materialerEt par nye undersøgelser viser, at to metallegeringer er i stand til at omdanne lys til elektrisk strøm effektivt takket være deres topologi. Denne grundlæggende forskning kan give en ny tilgang til u
Et nyt regime til analyse af egenskaber af topologiske materialerEt par nye undersøgelser viser, at to metallegeringer er i stand til at omdanne lys til elektrisk strøm effektivt takket være deres topologi. Denne grundlæggende forskning kan give en ny tilgang til u -
 Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a
Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a -
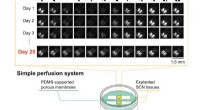 Hjernevæv holdt i live i ugevis på en kunstig membranNederst:mikroenhedsopsætningen med eksplanteret suprachiasmatic nucleus (SCN) væv. Øverst:rytmisk døgnaktivitet var stadig tydelig efter 25 dage, som angivet ved bioluminescensbilleddannelse. Kredit:R
Hjernevæv holdt i live i ugevis på en kunstig membranNederst:mikroenhedsopsætningen med eksplanteret suprachiasmatic nucleus (SCN) væv. Øverst:rytmisk døgnaktivitet var stadig tydelig efter 25 dage, som angivet ved bioluminescensbilleddannelse. Kredit:R
- Er RbBr en syre eller base?
- Hvad er de kemiske energikarakteristika?
- Hvad er 5 syrer og baser?
- Nyt design til nanopartikler, der absorberer lavenergilys, udsender højenergilys kan finde anvendel…
- Hvilke kationer kan bruges til at fremstille alunkrystaller?
- Nyt oliepalmekort til at informere om politik og planlægning på landskabsniveau


