Hvilken slags binding er resultatet overførsel af en elektron?
Her er hvorfor:
* Elektronoverførsel: I en ionisk binding mister et atom (typisk et metal) en elektron og bliver en positivt ladet ion (kation). Det andet atom (typisk en ikke -metal) vinder den elektron, der bliver en negativt ladet ion (anion).
* Elektrostatisk attraktion: De modsatte ladninger af kationen og anionen tiltrækker hinanden stærkt og skaber en stærk elektrostatisk kraft, der holder ionerne sammen i en krystalgitterstruktur.
Eksempel: I tabel salt (NaCl) mister natrium (NA) et elektron for at blive en natriumion (Na+), mens klor (CL) får, at elektronet bliver et chloridion (Cl-). Den elektrostatiske tiltrækning mellem disse modsatte ladede ioner skaber den ioniske binding, der danner natriumchlorid.
Sidste artikelHvor mange individuelle GE2CL6 -molekyler er der i en mol Ge2Cl6?
Næste artikelHvad er opløseligheden af et metal?
 Varme artikler
Varme artikler
-
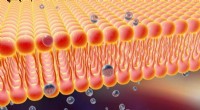 Fluorescerende prober beviser eksistensen af lipidflåde -cellemembranstrukturerKredit:Kyoto Universitet Forskere fra Japan, Indien og USA har for første gang observeret lipid-flåder i levende celler. Disse flåder er aktive sektioner af cellemembranen, der er ansvarlige for s
Fluorescerende prober beviser eksistensen af lipidflåde -cellemembranstrukturerKredit:Kyoto Universitet Forskere fra Japan, Indien og USA har for første gang observeret lipid-flåder i levende celler. Disse flåder er aktive sektioner af cellemembranen, der er ansvarlige for s -
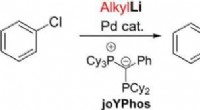 Direkte kobling af arylhalogenider og alkyllithiumforbindelser ved palladiumkatalyseKredit:Wiley Palladiumkatalysatorer hjælper med at syntetisere nøglekemikalier til mange industrier. Imidlertid, direkte reaktion af to grundlæggende reagenser, arylhalogenider og alkyllithiumforb
Direkte kobling af arylhalogenider og alkyllithiumforbindelser ved palladiumkatalyseKredit:Wiley Palladiumkatalysatorer hjælper med at syntetisere nøglekemikalier til mange industrier. Imidlertid, direkte reaktion af to grundlæggende reagenser, arylhalogenider og alkyllithiumforb -
 Sådan programmeres materialerAli Gooneie ser på en prøve fra sit seneste forskningsprojekt:elektrisk ledende polymerer. De første beregninger til hans næste projekt er skitseret på tavlen. Kredit:Empa Ali Gooneie simulerer på
Sådan programmeres materialerAli Gooneie ser på en prøve fra sit seneste forskningsprojekt:elektrisk ledende polymerer. De første beregninger til hans næste projekt er skitseret på tavlen. Kredit:Empa Ali Gooneie simulerer på -
 Gennembrud i organisk kemi:Asymmetriske synteser af nyttige, unikke chirale forbindelserSiden 2002 har et forskerhold, ledet af professor Osamu Kitagawa fra Shibaura Institute of Technology, har udviklet chirale Pd-katalyserede enantioselektive synteser for N-C aksialt chirale forbindels
Gennembrud i organisk kemi:Asymmetriske synteser af nyttige, unikke chirale forbindelserSiden 2002 har et forskerhold, ledet af professor Osamu Kitagawa fra Shibaura Institute of Technology, har udviklet chirale Pd-katalyserede enantioselektive synteser for N-C aksialt chirale forbindels
- Hvad ville der ske, hvis der er nogen videnskab?
- Tingenes internet via satellit bliver stadig mere tilgængelig
- Mand eller kvinde? Hos fluer kan nogle celler ikke fortælle det
- Indpakning af kobberterninger i nanostørrelse kan hjælpe med at omdanne kuldioxid til andre kemika…
- Hvad er lang tid mellem toppe i solfleksaktivitet?
- Hvilken type termiske energioverførsler forekommer for det meste i væsker?


