Vis ligningen af dissocieringsvand?
H₂O (L) ⇌ H⁺ (aq) + OH⁻ (aq)
Denne ligning repræsenterer følgende:
* h₂o (l): Flydende vandmolekyler.
* ⇌: Dette symbol indikerer, at reaktionen er reversibel, hvilket betyder, at det kan fortsætte i begge retninger.
* h⁺ (aq): Hydrogenioner (protoner) i vandig opløsning.
* OH⁻ (aq): Hydroxidioner i vandig opløsning.
Forklaring:
Vandmolekyler kan adskille sig i brintioner (H⁺) og hydroxidioner (OH⁻). Denne dissociation forekommer i meget lille grad, hvilket betyder, at kun en lille brøkdel af vandmolekyler ioniseres på ethvert givet tidspunkt. Dissociation er en ligevægtsproces, hvilket betyder, at de fremadgående og omvendte reaktioner forekommer med lige store hastigheder.
Vigtig note:
* Dissociation af vand er en vigtig faktor i bestemmelsen af dets pH. Rent vand har en pH på 7, som er neutral.
* Tilstedeværelsen af syrer eller baser kan skifte ligevægt af dissocieringsreaktionen, hvilket resulterer i en ændring i pH -værdien.
* Dissocieringskonstanten for vand (KW) er et mål for omfanget af dets dissociation. Ved 25 ° C er KW 1,0 × 10⁻¹⁴.
Sidste artikelHvad er dissocieringsligningen for Znf2?
Næste artikelEr kemiske forbindelser sammensat af et slags molekyle?
 Varme artikler
Varme artikler
-
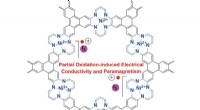 Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In
Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In -
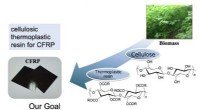 Elektronstråle styrker genanvendelig nanokompositFigur 1. Kulfiberforstærket plast med cellulosebaseret termoplast. Kredit:Kanazawa University Polymerer forstærket med kulfiber kombinerer styrke og lav vægt. De kan også prale af betydelige grønn
Elektronstråle styrker genanvendelig nanokompositFigur 1. Kulfiberforstærket plast med cellulosebaseret termoplast. Kredit:Kanazawa University Polymerer forstærket med kulfiber kombinerer styrke og lav vægt. De kan også prale af betydelige grønn -
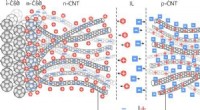 Forskere opdager overkommelig metode til produktion af transparente solcellerIonisk lukket lille-molekyle opv:grænseflade-doping af ladningssamler og transportlag. Kredit: ACS -anvendte materialer og grænseflader (2021). DOI:10.1021/acsami.0c17865 Fysikere fra ITMO Univ
Forskere opdager overkommelig metode til produktion af transparente solcellerIonisk lukket lille-molekyle opv:grænseflade-doping af ladningssamler og transportlag. Kredit: ACS -anvendte materialer og grænseflader (2021). DOI:10.1021/acsami.0c17865 Fysikere fra ITMO Univ -
 Se mor, ingen hænder:Forskere bruger vakuum til håndfri mønstre af flydende metalNorth Carolina State University ingeniører har brugt vakuum til at skabe en mere effektiv, håndfri metode til at fylde komplekse mikrokanaler med flydende metal. Deres arbejde adresserer to af de mest
Se mor, ingen hænder:Forskere bruger vakuum til håndfri mønstre af flydende metalNorth Carolina State University ingeniører har brugt vakuum til at skabe en mere effektiv, håndfri metode til at fylde komplekse mikrokanaler med flydende metal. Deres arbejde adresserer to af de mest


