Befri ikke metaller brintgas fra fortyndet. syrer?
Her er hvorfor:
* reaktionsmekanisme: Liberation af brintgas fra syrer forekommer typisk gennem en redox -reaktion . Et metalatom mister elektroner (oxidation) og bliver en positivt ladet ion, mens brintioner (H+) fra syreforstærkningselektroner (reduktion) for at danne brintgas (H2).
* ikke -metaller og oxidation: Ikke -metaller er generelt mere elektronegative end brint. Dette betyder, at de har en større tendens til at få elektroner, ikke miste dem. Derfor oxideres de ikke let for at danne positive ioner.
Eksempel:
* Metaller: Zink (Zn) reagerer med saltsyre (HCI) for at producere zinkchlorid (ZnCl2) og brintgas (H2):
`` `
Zn (S) + 2HCI (aq) → ZnCl2 (aq) + H2 (g)
`` `
* ikke -metaller: Svovl (er) reagerer ikke med fortyndet saltsyre. Det forbliver ureaktivt.
Undtagelser:
Der er nogle få undtagelser fra denne regel, hvor nogle ikke -metaller kan reagere med stærke oxidationssyrer (som koncentreret salpetersyre eller svovlsyre). Disse reaktioner er mere komplekse og involverer muligvis ikke frigørelse af brintgas.
Key Takeaway: Ikke -metaller fortrænger typisk ikke brint fra fortyndede syrer på grund af deres manglende reaktivitet i oxidationsprocesser.
Sidste artikelHvad er den kemiske formel NH4HSO4?
Næste artikelEr hældende væske en kemisk ændring eller fysisk?
 Varme artikler
Varme artikler
-
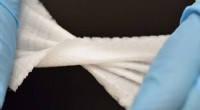 3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh
3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh -
 Forvandling af bilplastik til skum med kokosolieKredit:American Chemical Society Udtjente køretøjer, med deres plastik, metal- og gummikomponenter, er ansvarlige for millioner af tons affald rundt om i verden hvert år. Nu, et hold melder ind A
Forvandling af bilplastik til skum med kokosolieKredit:American Chemical Society Udtjente køretøjer, med deres plastik, metal- og gummikomponenter, er ansvarlige for millioner af tons affald rundt om i verden hvert år. Nu, et hold melder ind A -
 Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN
Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN -
 Identifikation af en ny, renere kilde til hvidt lysVed bestråling med infrarødt lys dannes adamantan-baserede molekylære klynger med den generelle sammensætning [(RT)4E5] (med R =organisk gruppe; T =C, Si, Ge, Sn; E =O, S, Se, Te, NH, CH2 , ON•) udsen
Identifikation af en ny, renere kilde til hvidt lysVed bestråling med infrarødt lys dannes adamantan-baserede molekylære klynger med den generelle sammensætning [(RT)4E5] (med R =organisk gruppe; T =C, Si, Ge, Sn; E =O, S, Se, Te, NH, CH2 , ON•) udsen
- Hvilken type reaaktion har altid ilt som reaktant?
- Tipforstærket Raman-spredning kan skelne mellem to strukturelt ens tilstødende molekyler
- Jordtyper i Temperate Løvfældende Skove
- Lavtlønsarbejdere i fare for automatisering:undersøgelse
- Opbevaring af mineaffald – sikkerhed er ingen tilfældighed, FN finder
- Amur-flodbassinet mistede 22% af sine vådområder fra 1980 til 2016


