Hvad sker der, når jernsulfatopløsning er opbevaret i aluminium?
reaktion:
Færrus sulfatopløsning reagerer med aluminiums -dåsen, hvilket fører til dannelse af aluminiumssulfat (Al₂ (SO₄) ₃) og metallisk jern (Fe). Denne reaktion er en enkelt forskydningsreaktion, hvor den mere reaktive aluminium erstatter jernet i jernsulfatet.
Kemisk ligning:
3Feso₄ (aq) + 2al (s) → Al₂ (so₄) ₃ (aq) + 3Fe (s)
Konsekvenser:
* Korrosion af aluminium kan: Aluminiumet kan korrodere, når det reagerer med jernsulfatopløsningen. Denne korrosion kan svække dåsen og føre til lækager eller endda fuldstændig fiasko.
* Dannelse af jernaflejringer: Jernen, der er dannet i reaktionen, vil deponere på indersiden af dåsen. Disse jernaflejringer kan påvirke kvaliteten af jernsulfatopløsningen, hvilket potentielt kan føre til forurening.
* Frigivelse af brintgas: I nogle tilfælde kan reaktionen også producere brintgas. Denne gas er brandfarlig og kan udgøre en sikkerhedsfare, hvis den bygger sig op i dåsen.
* Misfarvning af løsningen: Færrus sulfatopløsning kan blive misfarvet på grund af tilstedeværelsen af jernaflejringer og andre reaktionsprodukter.
Konklusion:
Opbevaring af jernsulfatopløsning i en aluminiums dåse anbefales ikke på grund af den kemiske reaktion, der forekommer, hvilket fører til korrosion, forurening og potentielle sikkerhedsfarer. Det er bedst at opbevare jernholdige sulfatopløsninger i containere lavet af materialer, der ikke er reaktive med opløsningen, såsom glas eller plast.
Sidste artikelHvor mange hydrogenatomer har 1 2 diaminopropan?
Næste artikelEr cyclopentan en væske eller gas ved stuetemperatur?
 Varme artikler
Varme artikler
-
 En opfindelse muliggør fremstilling af et naturligt sødemiddelKredit:Universitetet i Oulu En forskergruppe fra Oulu Universitet har udviklet en metode, der er i stand til at fremstille det naturlige sødestof brazzein. Produktion af brazzein som et velsmagend
En opfindelse muliggør fremstilling af et naturligt sødemiddelKredit:Universitetet i Oulu En forskergruppe fra Oulu Universitet har udviklet en metode, der er i stand til at fremstille det naturlige sødestof brazzein. Produktion af brazzein som et velsmagend -
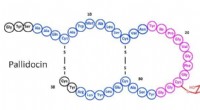 Nyt potent antimikrobielt middel fra termofil bakterieStrukturen af pallidocin, cirkler er aminosyreresterne, det funktionelle sukker ses til højre, knyttet til Cys. Kredit:Oscar Kuipers / University of Groningen Mikrobiologer fra University of Gro
Nyt potent antimikrobielt middel fra termofil bakterieStrukturen af pallidocin, cirkler er aminosyreresterne, det funktionelle sukker ses til højre, knyttet til Cys. Kredit:Oscar Kuipers / University of Groningen Mikrobiologer fra University of Gro -
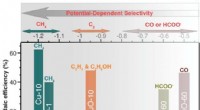 Selektive katalysatorer til kuldioxidgenanvendelseFigur viser, at selektiviteten af Cu-katalysatorer (ved fremstilling af specifikke kulstofbaserede forbindelser) bestemmes af den påførte spænding. Cu-10, CuO-1, CuO-10 og CuO-60 repræsenterer metal
Selektive katalysatorer til kuldioxidgenanvendelseFigur viser, at selektiviteten af Cu-katalysatorer (ved fremstilling af specifikke kulstofbaserede forbindelser) bestemmes af den påførte spænding. Cu-10, CuO-1, CuO-10 og CuO-60 repræsenterer metal -
 Forskere gør plastik mere nedbrydeligt under UV-lysKredit:Unsplash/CC0 Public Domain Mange plastiktyper, der er mærket som biologisk nedbrydelige, er kun komposterbare under industrielle forhold, men forskere ved University of Bath har nu fundet en
Forskere gør plastik mere nedbrydeligt under UV-lysKredit:Unsplash/CC0 Public Domain Mange plastiktyper, der er mærket som biologisk nedbrydelige, er kun komposterbare under industrielle forhold, men forskere ved University of Bath har nu fundet en
- Hvad forstår du ved bevægelsestilstand?
- Kortlægning af krystalformer kunne hurtigt spore 2D-materialer
- Hvem byggede det første rumskib?
- Hvordan kunne en blanding af sand og vand adskilles?
- Klimaændringer skaber ny risiko:Er indlandsbroer for lave?
- Mysterium om solcelledefekt løst efter årtiers global indsats


