Hvad er valensen af fluor?
Her er hvorfor:
* Elektronisk konfiguration: Fluor har 7 elektroner i sin yderste skal (2S² 2P⁵). Det har brug for endnu en elektron for at opnå en stabil oktetkonfiguration som Noble Gas Neon.
* At vinde elektroner: Fluor opnår denne stabilitet ved at få en elektron og danne en fluorion (F⁻). Denne forstærkning af en elektron gør sin valens 1.
Sidste artikelHvad er nikkel II -sulfat?
Næste artikelHvad er atommasse af benzen?
 Varme artikler
Varme artikler
-
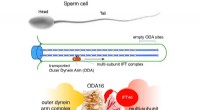 Transport af molekylære motorer til ciliaBilledet øverst viser en sædcelle med hoved (cellekrop) og hale (også kendt som flagellum eller cilium), der driver sædcellen fremad. Skemaet i midten viser, hvordan dyneinmotorer (gule stjerner) tran
Transport af molekylære motorer til ciliaBilledet øverst viser en sædcelle med hoved (cellekrop) og hale (også kendt som flagellum eller cilium), der driver sædcellen fremad. Skemaet i midten viser, hvordan dyneinmotorer (gule stjerner) tran -
 Biokemikere simulerer en proteinfoldende chaperones funktionel dansEt nyligt fremskridt i forståelsen af rollen som en interdomænelinker i Hsp70-chaperoner af Gieraschs gruppe ved UMass Amherst krævede smarte beregningsteknikker, massiv computerkraft og mesterlig b
Biokemikere simulerer en proteinfoldende chaperones funktionel dansEt nyligt fremskridt i forståelsen af rollen som en interdomænelinker i Hsp70-chaperoner af Gieraschs gruppe ved UMass Amherst krævede smarte beregningsteknikker, massiv computerkraft og mesterlig b -
 Forskere tilføjer orden til polymergelerEn prøve af den nye homogene polymergel. Kredit:© 2019 Li et al. Gel-lignende materialer har en lang række anvendelser, især inden for kemi og medicin. Imidlertid, deres anvendelighed er undertide
Forskere tilføjer orden til polymergelerEn prøve af den nye homogene polymergel. Kredit:© 2019 Li et al. Gel-lignende materialer har en lang række anvendelser, især inden for kemi og medicin. Imidlertid, deres anvendelighed er undertide -
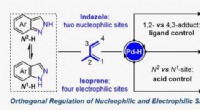 Ortogonal reguleringsstrategi giver nye muligheder for opbygning af molekylær kompleksitetPd-katalytisk regiodivergent dimethylallylering af indazol med isopren. Kredit:JIANG Wenshuang og JI Dingwei Dimethylallyl-relaterede enheder spiller en væsentlig rolle i at øge lipofilicitet af m
Ortogonal reguleringsstrategi giver nye muligheder for opbygning af molekylær kompleksitetPd-katalytisk regiodivergent dimethylallylering af indazol med isopren. Kredit:JIANG Wenshuang og JI Dingwei Dimethylallyl-relaterede enheder spiller en væsentlig rolle i at øge lipofilicitet af m
- Naturlige konserveringsmidler er i fremmarch
- Når antallet af atomer hver art på venstre side er en ligning lig med højre er?
- Ny strategi stabiliserer zink-ion-batterier
- Hvor mange atmosfæriske lag har solen?
- Hvad kalder vi brændstoffer, der kan produceres når som helst?
- Hvad er temaet for, da du hørte lært astronom?


