Når 2 farveløse væsker blandede sammen til at danne et lysegult fast stof, hvilke fysiske egenskaber har ændret sig?
* Farve: Dette er den mest åbenlyse ændring. Væskerne var farveløse, men det faste stof er lysegul. Dette indikerer en ændring i den måde, stoffet interagerer med lys på.
* Matterilat: Væskerne var i en flydende tilstand, og det faste stof er i en stiv tilstand. Dette er en betydelig ændring i arrangementet og bevægelsen af molekyler.
* opløselighed: Væskerne var sandsynligvis opløselige i hinanden (hvilket betyder, at de blandede). Det faste stof er sandsynligvis uopløseligt, hvilket indikerer en ændring i kræfterne mellem molekylerne.
* densitet: Densiteten af det faste stof vil være forskellig fra væskens densitet. Dette skyldes, at molekylerne er pakket tættere i et fast stof.
* smeltepunkt/frysepunkt: Det faste stof har et andet smeltepunkt (eller frysepunkt) end væskerne. Dette skyldes ændringerne i de intermolekylære kræfter, der holder molekylerne sammen.
mulige kemiske reaktioner
Denne proces involverer sandsynligvis en kemisk reaktion, hvor de to væsker reagerer for at danne en ny forbindelse. Denne nye forbindelse har en anden kemisk struktur, der giver den forskellige fysiske egenskaber.
Eksempler
Her er nogle eksempler på reaktioner, der kan føre til dannelse af et lysegult fast stof fra farveløse væsker:
* nedbørreaktioner: Blandingsløsninger indeholdende blyioner (PB²⁺) og iodidioner (I⁻) kan producere et lys gult bundfald af blyjodid (PBI₂).
* reaktioner, der involverer organiske forbindelser: Visse reaktioner, der involverer organiske forbindelser, såsom dannelse af et gult farvestof fra en reaktion af en farveløs væske med et andet kemikalie, kan føre til dette resultat.
For at forstå de specifikke fysiske egenskaber, der ændrede sig, har du brug for mere information om identiteten af de to farveløse væsker.
Sidste artikelHvorfor er vandmolekyle sfærisk?
Næste artikelHvad sker der, når svovldioxid opløst i vand testes af blåt lakmuspapir?
 Varme artikler
Varme artikler
-
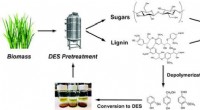 Vedvarende opløsningsmidler afledt af lignin sænker spild i biobrændstofproduktionBioraffinaderi-konceptet, der bruger fornybare dybe eutektiske opløsningsmidler (DES) afledt af ligninråvarer, er vist her. Kredit:US Department of Energy Et bioraffinaderi med lukket kredsløb kan
Vedvarende opløsningsmidler afledt af lignin sænker spild i biobrændstofproduktionBioraffinaderi-konceptet, der bruger fornybare dybe eutektiske opløsningsmidler (DES) afledt af ligninråvarer, er vist her. Kredit:US Department of Energy Et bioraffinaderi med lukket kredsløb kan -
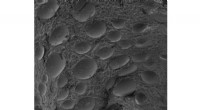 Ny polymer tackler PFAS -forureningForstørret visning af pulveriseret aktiveret kulpolymer, der binder sig til vandbåret PFAS, gør det muligt at fjerne det fra miljøet. Kredit:Flinders University Problemet med oprydning af giftige
Ny polymer tackler PFAS -forureningForstørret visning af pulveriseret aktiveret kulpolymer, der binder sig til vandbåret PFAS, gør det muligt at fjerne det fra miljøet. Kredit:Flinders University Problemet med oprydning af giftige -
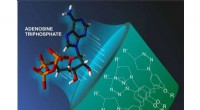 Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t -
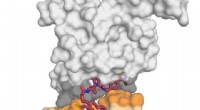 Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne
Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne


