Hvilken kemisk binding lagrer mest energi?
Her er hvorfor:
* obligationsstyrke: Triplebindinger involverer deling af seks elektroner mellem to carbonatomer. Dette skaber en meget stærk attraktion mellem atomerne, hvilket kræver en masse energi for at bryde bindingen.
* Energilagring: Jo højere bindingsstyrken, jo mere energi opbevares i bindingen.
Mens andre bindinger som C =O (carbonyl) eller C-H (carbon-hydrogen) også er vigtige i energilagring, pakker den tredobbelte binding i carbon-carbonbindinger den mest energi pr. Binding.
Eksempel: Energien, der er gemt i en C≡C-binding, er signifikant højere end for en C =C (dobbeltbinding) eller C-C (enkeltbinding). Dette er grunden til, at molekyler, der indeholder tredobbelte bindinger, som acetylen (C2H2), bruges som brændstoffer.
Sidste artikelHvad er elementerne til stede i almindeligt salt?
Næste artikelHvad er bidraget fra kemi i tøj?
 Varme artikler
Varme artikler
-
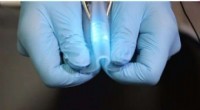 Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi
Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi -
 Ingeniører udvikler opskrifter til dramatisk at styrke kropsrustningenEt nærbillede af borkarbidkrystaller Kredit:Texas A&M University College of Engineering Ifølge gammel viden, Djengis Khan instruerede sine ryttere til at bære silkeveste under deres rustning for b
Ingeniører udvikler opskrifter til dramatisk at styrke kropsrustningenEt nærbillede af borkarbidkrystaller Kredit:Texas A&M University College of Engineering Ifølge gammel viden, Djengis Khan instruerede sine ryttere til at bære silkeveste under deres rustning for b -
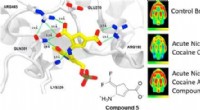 En forbedret medicin mod afhængighedKredit:American Chemical Society Narkotikamisbrug fortsætter med at plage et stort antal mennesker over hele verden, ødelægge og afslutte liv, mens forsøg på at udvikle mere effektive farmaceutisk
En forbedret medicin mod afhængighedKredit:American Chemical Society Narkotikamisbrug fortsætter med at plage et stort antal mennesker over hele verden, ødelægge og afslutte liv, mens forsøg på at udvikle mere effektive farmaceutisk -
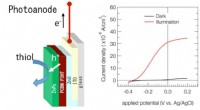 Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
- Hvordan varierer planetens tyngdekraft med deres masse?
- Hvad er en samling af økosystemer, der har det samme klima eller lignende dominerende samfund?
- Tilstedeværelsen af luftbåret støv kan betyde øget beboelighed af fjerne planeter
- Videresalg af billetmarkeder gavner sportshold og fans
- Nanodiamanter som fotokatalysatorer
- Kan du ikke se solformørkelsen? Lyt med online eller på tv


