Hvilke former, når noget opløses i en væske?
* opløst: Stoffet opløses (f.eks. Sukker, salt)
* opløsningsmiddel: Væsken gør opløsningen (f.eks. Vand)
* Løsning: Den homogene blanding dannet af det opløste opløste stof og opløsningsmidlet.
Sådan fungerer det:
1. opløsning: Solute -partiklerne går i stykker og bliver omgivet af opløsningsmiddelmolekyler. Denne proces er drevet af de attraktive kræfter mellem opløsningsmiddel- og opløsningsmiddelmolekylerne.
2. homogenitet: Den resulterende opløsning er homogen, hvilket betyder, at de opløste partikler er jævnt fordelt over opløsningsmidlet. Dette betyder, at løsningen har de samme egenskaber overalt.
Eksempler:
* sukker i vand: Sukker opløses i vand og danner en sukkeropløsning.
* salt i vand: Salt opløses i vand og danner en saltopløsning.
* te: Teblade opløses i varmt vand og danner en tesøsning.
Vigtig note: Ikke alle stoffer opløses i alle væsker. Et stofs evne til at opløses i en bestemt væske afhænger af arten af opløsningen og opløsningsmidlet. For eksempel opløses olie ikke i vand, men den opløses i benzin.
 Varme artikler
Varme artikler
-
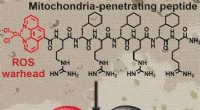 Et metallopeptid målretter og forstyrrer mitokondrielfunktionen i brystkræftstamcellerKredit:Wiley At dræbe maligne mitokondrier er en af de mest lovende fremgangsmåder i udviklingen af nye lægemidler mod kræft. Forskere fra Storbritannien har nu syntetiseret et kobberholdigt p
Et metallopeptid målretter og forstyrrer mitokondrielfunktionen i brystkræftstamcellerKredit:Wiley At dræbe maligne mitokondrier er en af de mest lovende fremgangsmåder i udviklingen af nye lægemidler mod kræft. Forskere fra Storbritannien har nu syntetiseret et kobberholdigt p -
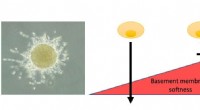 Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans
Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans -
 Team udvikler innovative, ideelle væskeafvisende overfladerProfessor Wang Liqui (til venstre) og Dr. Zhu Pingan fra HKU Mechanical Engineering Department fremviser det væskeafvisende materiale, de fornyede. Kredit:University of Hong Kong På væskeafvisende
Team udvikler innovative, ideelle væskeafvisende overfladerProfessor Wang Liqui (til venstre) og Dr. Zhu Pingan fra HKU Mechanical Engineering Department fremviser det væskeafvisende materiale, de fornyede. Kredit:University of Hong Kong På væskeafvisende -
 En ny proces til genanvendelse af metallurgisk slaggeKredit:CC0 Public Domain Forskere ved Ural Federal University (UrFU) og Institut for Metallurgi i Ural-afdelingen af Det Russiske Videnskabsakademi (UrB RAS) har udviklet og med succes testet te
En ny proces til genanvendelse af metallurgisk slaggeKredit:CC0 Public Domain Forskere ved Ural Federal University (UrFU) og Institut for Metallurgi i Ural-afdelingen af Det Russiske Videnskabsakademi (UrB RAS) har udviklet og med succes testet te
- Hvad er måderne har arbejdet omkring problemer med optiske teleskoper?
- Hvad er udtrykket til proces, hvor en del af gletsjeren bryder af og falder i vand?
- Hvad er arealet i kvadratmeter af 495 g Al-folie, der har en tykkelse på 29647 nm Densiteten 2,70 g…
- Hvad menes med en hydrofob aminosyre?
- Fristet til at snyde til en skriftlig eksamen? Kunstig intelligens er 90 % sikker på at fange dig
- Hvor mange inches er 30 mm?


