Vandmolekylet er polært, hvilket betyder, at hver ende af har en elektrisk ladning, fordi dette karakteristiske vand?
* Hydrogenbinding: Den positive ende af et vandmolekyle (hydrogenatomerne) tiltrækkes af den negative ende af et andet vandmolekyle (oxygenatomet). Disse attraktioner kaldes hydrogenbindinger. Hydrogenbindinger er relativt svage individuelt, men samlet gør de vand meget sammenhængende. Dette er grunden til, at vand har en høj overfladespænding, der giver ting som insekter mulighed for at gå på det.
* Høj specifik varme: På grund af brintbindingerne har vand brug for en masse energi for at hæve temperaturen. Dette gør vand til en fremragende temperaturregulator, der hjælper med at moderere Jordens klima og opretholde stabile indre temperaturer i levende organismer.
* universelt opløsningsmiddel: Vandets polaritet giver det mulighed for at opløse mange stoffer, inklusive salte og sukker. Dette skyldes, at de ladede ender af vandmolekyler kan omringe og adskille ladede molekyler, hvilket gør det til et vigtigt opløsningsmiddel for kemiske reaktioner i levende organismer.
* Densitetsanomali: Vand er mindre tæt som en fast (is) end som en væske. Dette skyldes, at hydrogenbindingen tvinger vandmolekyler til en mere åben, krystallinsk struktur i is. Dette er grunden til, at is flyder, som har vigtige konsekvenser for akvatisk liv og jordens klima.
Kort sagt er vandets polaritet grunden til, at det er et så unikt og vigtigt stof for livet, som vi kender det.
 Varme artikler
Varme artikler
-
 Forskere udvikler den første funktionelle ikke-native metalhydrogenaseKredit:CC0 Public Domain Hydrogenaser er enzymer, der katalyserer hydrogenaktivering. Der er tre typer hydrogenaser i naturen, alle indeholder jern og nogle af dem nikkel. Men i syntetisk kemi er
Forskere udvikler den første funktionelle ikke-native metalhydrogenaseKredit:CC0 Public Domain Hydrogenaser er enzymer, der katalyserer hydrogenaktivering. Der er tre typer hydrogenaser i naturen, alle indeholder jern og nogle af dem nikkel. Men i syntetisk kemi er -
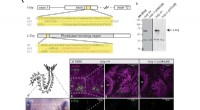 Lysfølsomt molekyle hjælper havdyr med at synkronisere deres reproduktionscyklusl-cry–/– mutanter er alleler med tab af funktion. en oversigt over det genomiske l-cry-locus for wt og mutanter. Begge mutante alleler resulterer i et tidligt rammeskift og for tidlige stopkodoner. Δ3
Lysfølsomt molekyle hjælper havdyr med at synkronisere deres reproduktionscyklusl-cry–/– mutanter er alleler med tab af funktion. en oversigt over det genomiske l-cry-locus for wt og mutanter. Begge mutante alleler resulterer i et tidligt rammeskift og for tidlige stopkodoner. Δ3 -
 En metode til at erstatte nedbrudt perovskit i solceller, hvilket gør dem genanvendeligeDen tredobbelte oxid mesoporøse indiumtinoxid perovskit-baserede solcellestruktur. Kredit:Avi Schneider. Et team af forskere ved det hebraiske universitet i Jerusalem har udviklet en teknik til fr
En metode til at erstatte nedbrudt perovskit i solceller, hvilket gør dem genanvendeligeDen tredobbelte oxid mesoporøse indiumtinoxid perovskit-baserede solcellestruktur. Kredit:Avi Schneider. Et team af forskere ved det hebraiske universitet i Jerusalem har udviklet en teknik til fr -
 Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt
Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt
- Ekstremerne i klimaet er nøglefaktoren bag stigende global sult:FN
- Hvad er forskellen mellem erosion og afsætning?
- Hvordan man demonstrerer Newtons love om bevægelse
- Kangaroo Island viser forbrændingsar på en tredjedel af landmassen
- Sådan beregnes vægt pr. Lineær fod
- Hvilken indflydelse havde Galileo på den moderne Wolrd?


