Hvorfor klor fortrænger brom fra kaliumbromid?
* Elektronegativitet: Klor er mere elektronegativ end brom. Dette betyder, at klor har en stærkere attraktion for elektroner.
* reaktivitet: Højere elektronegativitet oversætter til større reaktivitet. Chlor, der er mere reaktiv, trækker let elektroner væk fra brom i kaliumbromidforbindelsen.
* reaktion: Reaktionen mellem klor og kaliumbromid er en enkelt forskydningsreaktion:
cl₂ (g) + 2kbr (aq) → 2kcl (aq) + br₂ (l)
* Chlor (CL₂) reagerer med kaliumbromid (KBR).
* Chlor indtager stedet for brom i forbindelsen og danner kaliumchlorid (KCL).
* Brom (Br₂) frigives som en væske.
I det væsentlige tillader klorens stærkere træk på elektroner at "sparke" brom fra forbindelsen og danne en ny forbindelse med kalium. Denne reaktion er drevet af elementernes tendens til at opnå en mere stabil elektronkonfiguration.
Sidste artikelEr KBR en forbindelse eller fast?
Næste artikelHvad er kombinationsforholdet mellem kalium og brom?
 Varme artikler
Varme artikler
-
 Direkte observation af desorption af en smelte af lange polymerkæderKredit:CC0 Public Domain I vores hverdag er det ikke ualmindeligt at se det samme materiale i forskellige tilstande. Tag for eksempel vand:det er en væske ved omgivelsestemperatur, vi kan omdanne
Direkte observation af desorption af en smelte af lange polymerkæderKredit:CC0 Public Domain I vores hverdag er det ikke ualmindeligt at se det samme materiale i forskellige tilstande. Tag for eksempel vand:det er en væske ved omgivelsestemperatur, vi kan omdanne -
 Fødevareforskere skaber sunde probiotiske drik fra sojapulpLektor Shao-Quan Liu og ph.d.-studerende Weng-Chan Vong fra NUS Food Science and Technology Program har udtænkt en unik cocktail af enzymer, probiotika og gær til at producere en okara-drik rig på tar
Fødevareforskere skaber sunde probiotiske drik fra sojapulpLektor Shao-Quan Liu og ph.d.-studerende Weng-Chan Vong fra NUS Food Science and Technology Program har udtænkt en unik cocktail af enzymer, probiotika og gær til at producere en okara-drik rig på tar -
 En ny metode til kvantitativ vurdering af graden af lighed af koordineringspolyederTrekanterne angiver CPerne svarende til trigonal bipyramid, og de åbne og grå firkanter angiver tetragonal pyramide med det centrale atom i basen og i centrum af massen, henholdsvis. Kredit:Lobachevsk
En ny metode til kvantitativ vurdering af graden af lighed af koordineringspolyederTrekanterne angiver CPerne svarende til trigonal bipyramid, og de åbne og grå firkanter angiver tetragonal pyramide med det centrale atom i basen og i centrum af massen, henholdsvis. Kredit:Lobachevsk -
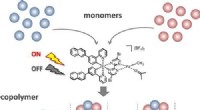 Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr
Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr
- Hvilke typer reaktioner forekommer i en stjerne?
- Under klassificeringssystem i øjeblikket i brug Hvordan organiserer forskere data om levende ting?
- Hvornår begyndte den precambriske tid?
- Hvordan hologrammer virker
- Hvilken procentdel af energi kommer fra fossile brændstoffer i USA?
- Er det at se tro? Egentlig ikke, så dyrevelfærdskampagner bør tage en anden tilgang


