Laves CO2 et molekylært fast stof?
* molekylære faste stoffer dannes af molekyler, der holdes sammen af intermolekylære kræfter (som van der Waals -kræfter eller hydrogenbinding). Disse kræfter er relativt svage.
* kovalente netværksstoffer dannes af atomer, der er knyttet sammen af et kontinuerligt netværk af stærke kovalente bindinger.
I tilfælde af CO2:
* Hvert carbonatom i CO2 danner dobbeltbindinger med to iltatomer.
* Disse obligationer er stærke kovalente obligationer.
* De resulterende CO2 -molekyler har en lineær form, og de interagerer kun med hinanden gennem svage van der Waals -styrker.
* Ved meget lave temperaturer (under -78 ° C) arrangerer CO2 -molekyler sig i en specifik, ordnet struktur, hvor carbonatomerne er knyttet til hinanden gennem svage van der Waals -styrker. Denne ordning betragtes stadig som et molekylært fast stof, men det er ikke den typiske tilstand af CO2 ved stuetemperatur.
Mens CO2 derfor danner et molekylært fast stof ved meget lave temperaturer, beskrives det mere nøjagtigt som et kovalent netværksstof Ved stuetemperatur på grund af de stærke kovalente bindinger inden for CO2 -molekylerne.
Sidste artikelHvorfor kombineres to atomer?
Næste artikelVil jernpulver opløses i vand?
 Varme artikler
Varme artikler
-
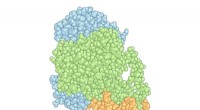 Forskere undersøger måder, hvorpå et lægemiddel som Avandia kan gøres mere sikkertKomplekset af PPARγ (grøn) og RXRα (blå) med DNA (orange). Kredit:Scripps Research Institute Med de øgede bekymringer over de farlige bivirkninger af det engang populære antidiabetika, Avandia, fo
Forskere undersøger måder, hvorpå et lægemiddel som Avandia kan gøres mere sikkertKomplekset af PPARγ (grøn) og RXRα (blå) med DNA (orange). Kredit:Scripps Research Institute Med de øgede bekymringer over de farlige bivirkninger af det engang populære antidiabetika, Avandia, fo -
 Eliminerer revner i 3-D-printede metalkomponenterKredit:istock Forskere ved EPFL har udviklet en ny laser 3-D-printteknik til fremstilling af metalkomponenter med hidtil uset modstandsdygtighed over for høje temperaturer, skader og korrosion. Me
Eliminerer revner i 3-D-printede metalkomponenterKredit:istock Forskere ved EPFL har udviklet en ny laser 3-D-printteknik til fremstilling af metalkomponenter med hidtil uset modstandsdygtighed over for høje temperaturer, skader og korrosion. Me -
 Frigør potentialet for metalnanopartikler som katalysatorer for hurtig og effektiv CO2-omdannelseNano-arkitektur:nikkelpartikler præcis 1/40, 000. på størrelse med et menneskehår er de bedste katalysatorer til omdannelse af CO2. Kredit:Utrecht University / Uorganisk kemi og katalyse O 2 og
Frigør potentialet for metalnanopartikler som katalysatorer for hurtig og effektiv CO2-omdannelseNano-arkitektur:nikkelpartikler præcis 1/40, 000. på størrelse med et menneskehår er de bedste katalysatorer til omdannelse af CO2. Kredit:Utrecht University / Uorganisk kemi og katalyse O 2 og -
 Brændstof ud af den blå luft:Ny vej til opsamling og opgradering af CO2Geonhui Lee, Ph.d. -kandidat, driver en elektrolysator, der er i stand til at omdanne opløst carbonat til CO2 og derefter til syngas. Enheden tilbyder en ny, kortere vej til omdannelse af atmosfærisk
Brændstof ud af den blå luft:Ny vej til opsamling og opgradering af CO2Geonhui Lee, Ph.d. -kandidat, driver en elektrolysator, der er i stand til at omdanne opløst carbonat til CO2 og derefter til syngas. Enheden tilbyder en ny, kortere vej til omdannelse af atmosfærisk
- Lys (fysik): Hvad er det og hvordan fungerer det?
- Forvent færre, men mere destruktive landfaldende tropiske cykloner
- Hvad stammer ordet geotermisk fra?
- Hvilke faktorer påvirker stærkest den type biome, der dannes på et bestemt sted på land?
- Vejledning af en superledende fremtid med grafenkvantemagi
- De sidste 25 %:Sådan tackler du svært tilgængelige emissioner


