Hvor mange K -ioner ain 6,76 mol K3PO4?
1. Forstå formlen:
* K₃po₄ repræsenterer kaliumphosphat.
* Underskriften "3" i k₃po₄ indikerer, at der er 3 kalium (k) ioner for hver 1 formelenhed for kaliumphosphat.
2. Brug Avogadros nummer:
* Avogadros nummer fortæller os, at der er 6,022 x 10²³ partikler (atomer, molekyler, ioner osv.) I en mol af et stof.
3. Beregn antallet af K -ioner:
* Trin 1: Find molen af k -ioner:Da der er 3 mol k -ioner for hver 1 mol k₃po₄, har vi 6,76 mol k₃po₄ * (3 mol k / 1 mol k₃po₄) =20,28 mol k k
* Trin 2: Konverter mol af K -ioner til antal K -ioner:20,28 mol K * (6,022 x 10²³ K -ioner/mol K) =1,22 x 10²⁵ K -ioner
Derfor er der cirka 1,22 x 10²⁵ kaliumioner i 6,76 mol k₃po₄.
Sidste artikelHvordan er alle atomer af jern forskellige fra de andre elementer?
Næste artikelEr C3H6BR2 polær eller ikke polær?
 Varme artikler
Varme artikler
-
 Fysiker skaber N95-type åndedrætsværn ved hjælp af en bomuldsmaskineKredit:Pixabay/CC0 Public Domain Mahesh Bandi, en fysiker med den ikke-lineære og ikke-ligevægtsfysikenhed, OIST Graduate University, Onna, Okinawa, har fundet en måde at fremstille N95-type respi
Fysiker skaber N95-type åndedrætsværn ved hjælp af en bomuldsmaskineKredit:Pixabay/CC0 Public Domain Mahesh Bandi, en fysiker med den ikke-lineære og ikke-ligevægtsfysikenhed, OIST Graduate University, Onna, Okinawa, har fundet en måde at fremstille N95-type respi -
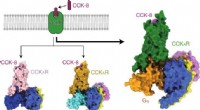 Mekanisme af virkninger af cholecystokinin-receptorer afsløretGrafisk abstrakt. Kredit:DOI:10.1038/s41589-021-00841-3 Cholecystokinin (CCK) og gastrin er de tidligst opdagede gastrointestinale hormoner. De er de mest udbredte peptider i mave-tarmkanalen og c
Mekanisme af virkninger af cholecystokinin-receptorer afsløretGrafisk abstrakt. Kredit:DOI:10.1038/s41589-021-00841-3 Cholecystokinin (CCK) og gastrin er de tidligst opdagede gastrointestinale hormoner. De er de mest udbredte peptider i mave-tarmkanalen og c -
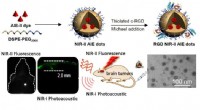 Ny metode hjælper med at gøre ortotopisk hjerne-tumor-billeddannelse klarere og hurtigereNIR-II fluorescerende molekyle med aggregeringsinduceret emission (AIE) brugt til ortotopisk hjernetumorbilleddannelse. Kredit:ZHENG Hairong I øjeblikket, tumorer inde i centralnervesystemet er bl
Ny metode hjælper med at gøre ortotopisk hjerne-tumor-billeddannelse klarere og hurtigereNIR-II fluorescerende molekyle med aggregeringsinduceret emission (AIE) brugt til ortotopisk hjernetumorbilleddannelse. Kredit:ZHENG Hairong I øjeblikket, tumorer inde i centralnervesystemet er bl -
 Udfordringer i udviklingen af elektrokatalysatorerKredit:Pixabay/CC0 Public Domain Regenerativ energihøst genererer ofte mere elektricitet, end der er behov for direkte. Elektrokemiske processer kunne bruges til at lagre den overskydende energi e
Udfordringer i udviklingen af elektrokatalysatorerKredit:Pixabay/CC0 Public Domain Regenerativ energihøst genererer ofte mere elektricitet, end der er behov for direkte. Elektrokemiske processer kunne bruges til at lagre den overskydende energi e
- Hvorfor er USA ikke et godt sted for luftmasser at danne?
- Hvor produceres de fleste af planter xylem og floem?
- Google muliggør brug af Android -telefoner som en fysisk sikkerhedsnøgle
- Bekæmpelse af kræft ved nulpunktet med designermolekyler
- Er svovldioxid et grundlæggende oxid?
- Stjernemord:Når stjerner ødelægger og spiser deres egne planeter


