Hvordan ville du forberede en 300 ml 0,1 m Na Cl -opløsning fra fast og vand?
1. Beregn den nødvendige masse af NaCl:
* Molær masse af NaCl: 58,44 g/mol
* ønsket koncentration: 0,1 m (mol pr. Liter)
* bind: 300 ml =0,3 L
* Formel: masse (g) =koncentration (mol/l) x volumen (l) x molær masse (g/mol)
* Beregning: masse =0,1 mol/l * 0,3 L * 58,44 g/mol =1,7532 g
2. Vej ud NaCl:
* Brug en analytisk balance til nøjagtigt at afveje 1.7532 g NaCl.
3. Opløs NaCl i vand:
* Tilsæt NaCl til en ren, tør 300 ml volumetrisk kolbe.
* Tilsæt en lille mængde destilleret vand (ca. 100 ml) til kolben og hvirvle forsigtigt for at opløse NaCl helt.
* Tilsæt mere destilleret vand, indtil kolben er omkring tre fjerdedele fuld.
* Tilsæt forsigtigt destilleret vand til mærket på halsen på den volumetriske kolbe.
* Stopper kolben og vend den flere gange for at sikre grundig blanding.
Vigtige noter:
* Brug destilleret vand: Destilleret vand er fri for urenheder, der kan påvirke koncentrationen af din opløsning.
* nøjagtig vejning: Brug en analytisk balance for at sikre, at du vejer NaCl nøjagtigt.
* Volumetrisk kolbe: Brug en volumetrisk kolbe for at sikre præcis volumenmåling.
* Bland grundigt: Inverter kolben flere gange efter opløsning af NaCI for at sikre en homogen opløsning.
Mærkning:
* Mærk løsningen tydeligt med koncentrationen (0,1 m), opløstelsen (NaCl), datoen og dit navn eller initialer.
sikkerhed:
* Brug altid beskyttelsesbriller og handsker, når du håndterer kemikalier.
* Arbejd i et godt ventileret område.
* Bortskaf løsningen korrekt i henhold til dit laboratories retningslinjer.
 Varme artikler
Varme artikler
-
 Roamingreaktioner undersøger at kaste nyt lys over atmosfæriske molekylerKredit:CC0 Public Domain En detaljeret undersøgelse af roamingreaktioner - hvor atomer af forbindelser deler sig og kredser om andre atomer for at danne uventede nye forbindelser - kunne sætte for
Roamingreaktioner undersøger at kaste nyt lys over atmosfæriske molekylerKredit:CC0 Public Domain En detaljeret undersøgelse af roamingreaktioner - hvor atomer af forbindelser deler sig og kredser om andre atomer for at danne uventede nye forbindelser - kunne sætte for -
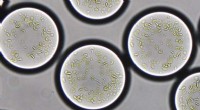 Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e
Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e -
 Video:Sådan får kimchi sit kickKredit:The American Chemical Society Kimchi, den fermenterede kålskål, der er elsket i Korea og rundt om i verden, har en signatur skarp, sur tang. Disse unikke smag kommer fra ikke kun salt og k
Video:Sådan får kimchi sit kickKredit:The American Chemical Society Kimchi, den fermenterede kålskål, der er elsket i Korea og rundt om i verden, har en signatur skarp, sur tang. Disse unikke smag kommer fra ikke kun salt og k -
 Forskere afslører en hemmelighed bag stærkere metallerFor første gang har forskere beskrevet, hvordan de små krystallinske korn, der udgør de fleste faste metaller, faktisk dannes. At forstå denne proces, siger de, kunne teoretisk set føre til måder at p
Forskere afslører en hemmelighed bag stærkere metallerFor første gang har forskere beskrevet, hvordan de små krystallinske korn, der udgør de fleste faste metaller, faktisk dannes. At forstå denne proces, siger de, kunne teoretisk set føre til måder at p
- Billede:Hubble finder Medusa på himlen
- Hvilke 2 fysiske egenskaber kan bruges til at adskille ethanol og vand?
- Hvad betyder genetisk identisk?
- Nyt lasergennembrud for at hjælpe med forståelsen af gravitationsbølger
- Hvordan laver man en hjemmelavet hoppekugle lavet af et æg
- Hvilke to faktorer bestemmer, hvor lys en stjerne ser ud fra jorden?


