Hvad skulle der få to elektroner for at opnå det samme antal som en ædel gas o eller sr na se br?
* Forståelse af ædelgaskonfiguration: Ædle gasser har en fuld ydre skal af elektroner, hvilket gør dem meget stabile. Atomer har en tendens til at vinde eller miste elektroner for at opnå denne stabile konfiguration.
* analyse af elementerne:
* o (ilt): Oxygen har 6 elektroner i sin ydre skal. Det skal vinde to Elektroner for at opnå den stabile elektronkonfiguration af neon (NE).
* sr (strontium): Strontium har 2 elektroner i sin ydre skal. Det mister to Elektroner for at opnå den stabile elektronkonfiguration af Krypton (KR).
* na (natrium): Natrium har 1 elektron i sin ydre skal. Det mister en Elektron for at opnå den stabile elektronkonfiguration af Neon (NE).
* se (selen): Selen har 6 elektroner i sin ydre skal. Det skal vinde to Elektroner for at opnå den stabile elektronkonfiguration af Krypton (KR).
* br (brom): Bromin har 7 elektroner i sin ydre skal. Det skal vinde en Elektron for at opnå den stabile elektronkonfiguration af Krypton (KR).
Derfor er de elementer, der skulle få to elektroner for at opnå det samme antal elektroner som en ædelgas, ilt (O) og selen (SE).
 Varme artikler
Varme artikler
-
 Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g
Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g -
 Ny måde at forvandle nummer syv plastik til værdifulde produkterWSU-forskerholdet, inklusive postdoc-forsker Yu-Chung Chang, brugte PLA-plastaffald til at skabe en højkvalitets harpiks til 3D-print. Kredit:WSU En metode til at konvertere en almindeligt smidt pl
Ny måde at forvandle nummer syv plastik til værdifulde produkterWSU-forskerholdet, inklusive postdoc-forsker Yu-Chung Chang, brugte PLA-plastaffald til at skabe en højkvalitets harpiks til 3D-print. Kredit:WSU En metode til at konvertere en almindeligt smidt pl -
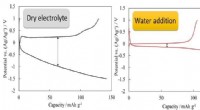 Elektrolyttens struktur styrer batteriets ydeevneVi har fundet ud af, at tilsætning af vand i høj grad reducerer forskellen i spænding (overspænding) mellem opladning/afladning. Kredit:COPYRIGHT (C) TOYOHASHI UNIVERSITY OF TECHNOLOGY. Forskerhol
Elektrolyttens struktur styrer batteriets ydeevneVi har fundet ud af, at tilsætning af vand i høj grad reducerer forskellen i spænding (overspænding) mellem opladning/afladning. Kredit:COPYRIGHT (C) TOYOHASHI UNIVERSITY OF TECHNOLOGY. Forskerhol -
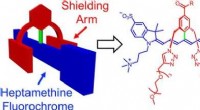 Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de
Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de
- Hvem opdagede, at elektroner rejser i visse stier eller energiniveau?
- Hvad er området med Continental USA?
- Hvordan tester man, om væsken er destilleret vand eller postevand?
- Langt søgt proteinstruktur kan hjælpe med at afsløre, hvordan 'genskift' virker (video)
- Vil omdøbning af carp copi hjælpe med at kontrollere dem?
- Trump beder NASA om at sende amerikanere til Månen


