Hvad forekommer når salt jævnt blandet med vand?
* opløsning: Saltkrystaller opløses i deres individuelle ioner:natriumioner (Na+) og chloridioner (Cl-). Dette sker, fordi vandmolekyler er polære, hvilket betyder, at de har en lidt positiv ende og en lidt negativ ende. Disse polære molekyler tiltrækker de ladede ioner af saltet, trækker dem fra hinanden og omgiver dem.
* Dannelse af en løsning: De opløste ioner spredes nu jævnt i hele vandet, hvilket skaber en homogen blanding kaldet en opløsning.
* Forøgelse i ledningsevne: Tilstedeværelsen af ionerne i opløsningen giver den mulighed for at udføre elektricitet. Rent vand er en dårlig dirigent, men tilsætning af salt gør det til en meget bedre dirigent.
* sænkning af frysepunkt: Tilsætning af salt til vand sænker temperaturen, hvormed den fryser. Dette er grunden til, at salt bruges på veje og fortove til at smelte is.
* hævning af kogepunkt: Vandets kogepunkt hæves også, når salt tilsættes. Dette er grunden til, at salt bruges til madlavning for at øge temperaturen på kogende vand.
* Ændringer i osmotisk tryk: Tilstedeværelsen af opløste ioner ændrer opløsningens osmotiske tryk, hvilket kan være vigtigt i biologiske systemer.
Generelt, når salt blandes jævnt med vand, opløses det og skaber en salt opløsning med forskellige fysiske og kemiske egenskaber end rent vand.
Sidste artikelHvilke kemikere kan sige, at reaktanter produkter?
Næste artikelHvor skjult PPM til pH?
 Varme artikler
Varme artikler
-
 En opdateret forståelse af, hvordan man syntetiserer værdiskabende kemikalierKredit:CC0 Public Domain Forskere har længe været interesseret i at finde måder at bruge simple kulbrinter på, kemikalier lavet af et lille antal kulstof- og brintatomer, at skabe værdiskabende ke
En opdateret forståelse af, hvordan man syntetiserer værdiskabende kemikalierKredit:CC0 Public Domain Forskere har længe været interesseret i at finde måder at bruge simple kulbrinter på, kemikalier lavet af et lille antal kulstof- og brintatomer, at skabe værdiskabende ke -
 Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin
Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin -
 Forskere genskaber parfume fra det 17. århundrede af Constantijn HuygensEn krukke med ingredienserne til parfumen. Kredit:Leiden University Et team af forskere fra Young Academy og Huygens ING/NL Lab har bragt en tre århundreder gammel duft til live baseret på en opskr
Forskere genskaber parfume fra det 17. århundrede af Constantijn HuygensEn krukke med ingredienserne til parfumen. Kredit:Leiden University Et team af forskere fra Young Academy og Huygens ING/NL Lab har bragt en tre århundreder gammel duft til live baseret på en opskr -
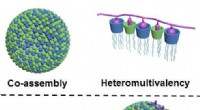 Kemikere udvikler ny metode til selektiv binding af proteinerFigur øverst:Gennem sammontering, to komponenter af lipidtypen danner nano-partikler i vand, som har et meget stort antal forskellige kontaktpunkter (vist med blå og grøn; til venstre). Som et resulta
Kemikere udvikler ny metode til selektiv binding af proteinerFigur øverst:Gennem sammontering, to komponenter af lipidtypen danner nano-partikler i vand, som har et meget stort antal forskellige kontaktpunkter (vist med blå og grøn; til venstre). Som et resulta
- Ingeniører øger effektiviteten til at omdanne drivhusgas til ethylen
- Enzymboost kan fremskynde produktionen af biobrændstoffer og andre bioforarbejdede materialer
- De planeter, der er kendt som gasgiganter, inkluderer?
- Forskere lader frem for at udvikle bedre batterier
- Hvad er sikkerhedsretningslinjerne for interaktiv videnskabsnotatbog?
- Ribosomernes rolle i homeostasis


