Hvorfor er methan -dipolmomentet nul?
1. tetrahedral geometri: Metan har et centralt carbonatom bundet til fire hydrogenatomer, arrangeret i en tetrahedral form. Dette betyder, at de fire C-H-bindinger peger mod hjørnerne af en tetrahedron med bindingsvinkler på ca. 109,5 grader.
2. lige elektronegativitet: Carbon og brint har lignende elektronegativiteter. Dette betyder, at elektronerne i C-H-bindingerne deles næsten lige mellem de to atomer.
3. symmetri: På grund af den tetrahedrale geometri er de fire C-H-bindinger arrangeret symmetrisk omkring carbonatomet. Dette betyder, at elektrondensiteten er jævnt fordelt omkring molekylet, hvilket resulterer i intet netto dipolmoment.
Tænk på det sådan:
Forestil dig fire personer, der trækker på et reb fra hvert hjørne af en firkant. Hvis de trækker med lige kraft, bevæger rebet ikke i nogen bestemt retning. Tilsvarende trækker de fire C-H-bindinger i metan på elektrondensiteten lige i alle retninger, hvilket resulterer i intet netto dipolmoment.
I modsætning hertil har molekyler som vand (H₂O) et dipolmoment, fordi iltatomet er mere elektronegativt end brint, hvilket resulterer i en skæv elektronfordeling og et netto dipolmoment.
 Varme artikler
Varme artikler
-
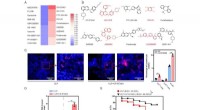 PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre)
PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre) -
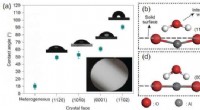 Safirer viser deres sande farver:Ikke vandelskendeMakroskopiske befugtningsforskelle af forskellige α-Al2O3 krystalflader og skematiske diagrammer for at illustrere mekanismen på molekylært niveau. (a) Polykrystallinsk aluminiumoxid er meget hydrofil
Safirer viser deres sande farver:Ikke vandelskendeMakroskopiske befugtningsforskelle af forskellige α-Al2O3 krystalflader og skematiske diagrammer for at illustrere mekanismen på molekylært niveau. (a) Polykrystallinsk aluminiumoxid er meget hydrofil -
 Forskere udvikler ikke-ædellegeringskatalysator til kanelaldehyd(en). Skematisk illustration af synteseproceduren for FeXCo@NC; (b). TEM-billede (indsæt:TEM-billede med høj forstørrelse og Fe-Co NPs størrelsesfordeling); (c) XRD-mønster; (d-e) HAADF-STEM, tilsvare
Forskere udvikler ikke-ædellegeringskatalysator til kanelaldehyd(en). Skematisk illustration af synteseproceduren for FeXCo@NC; (b). TEM-billede (indsæt:TEM-billede med høj forstørrelse og Fe-Co NPs størrelsesfordeling); (c) XRD-mønster; (d-e) HAADF-STEM, tilsvare -
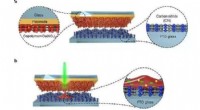 Nanomaterialer med laserprintSådan fungerer den nye laserdrevne metode. Kredit:Max Planck Institute of Colloids and Interfaces I journalen Naturkommunikation , et tværfagligt team fra Max Planck Institute of Colloids and In
Nanomaterialer med laserprintSådan fungerer den nye laserdrevne metode. Kredit:Max Planck Institute of Colloids and Interfaces I journalen Naturkommunikation , et tværfagligt team fra Max Planck Institute of Colloids and In


