Bestemer farven på et element atomer elektronegativitet?
Her er hvorfor:
* Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding. Det bestemmes af faktorer som antallet af protoner i kernen (højere antal =stærkere træk) og afstanden til valenselektroner fra kernen (tættere =stærkere træk).
* farve bestemmes af den måde, et element interagerer med lys. Elektroner absorberer og udsender specifikke bølgelængder af lys, hvilket resulterer i den farve, vi opfatter. Dette påvirkes af elementets elektroniske struktur, men ikke direkte relateret til elektronegativitet.
Eksempel:
* guld er et skinnende gult metal. Dens farve skyldes, hvordan dens elektroner interagerer med lys. Imidlertid har guld en relativt lav elektronegativitet sammenlignet med andre elementer.
* fluor er en lysegul gas. Mens den har en lignende farve som guld, har fluor den højeste elektronegativitet af alle elementer.
Kortfattet: Mens farve og elektronegativitet begge er relateret til et elements elektroniske struktur, bestemmes de af forskellige aspekter af denne struktur.
Sidste artikelOpløses enkle kulhydrater i vand?
Næste artikelHvad er et molekyle med den generelle formel CH2O?
 Varme artikler
Varme artikler
-
 Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels
Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels -
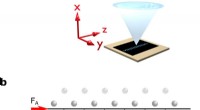 Laserkølede ioner bidrager til bedre forståelse af friktiona) 30 ytterbium-ioner fanges i en lineær radiofrekvensfælde. Laser 1 bestråler hele krystallen og får den til at fluorescere. Dette lys opsamles ved hjælp af et objektiv i høj opløsning og afbildes på
Laserkølede ioner bidrager til bedre forståelse af friktiona) 30 ytterbium-ioner fanges i en lineær radiofrekvensfælde. Laser 1 bestråler hele krystallen og får den til at fluorescere. Dette lys opsamles ved hjælp af et objektiv i høj opløsning og afbildes på -
 Ligesom Wolverine, mennesker har brug for metal for at opretholde stærke knoglerKredit:University of Manchester Et internationalt team af forskere, ledet af University of Manchester, har brugt det britiske Diamond Light Source-anlæg (billedet ovenfor) til at afbilde den præci
Ligesom Wolverine, mennesker har brug for metal for at opretholde stærke knoglerKredit:University of Manchester Et internationalt team af forskere, ledet af University of Manchester, har brugt det britiske Diamond Light Source-anlæg (billedet ovenfor) til at afbilde den præci -
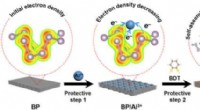 Regulering af reaktiviteten af sort fosfor gennem beskyttende kemiSkematisk illustration af regulering af reaktiviteten af BP via beskyttende kemi. Beskyttelsestrin 1:Binding af Al3+ ioner med ensomme elektronpar på overfladen af P-atomer reducerer overfladeelek
Regulering af reaktiviteten af sort fosfor gennem beskyttende kemiSkematisk illustration af regulering af reaktiviteten af BP via beskyttende kemi. Beskyttelsestrin 1:Binding af Al3+ ioner med ensomme elektronpar på overfladen af P-atomer reducerer overfladeelek
- Hvor er elementer med det samme antal valenselektroner?
- En miniaturestrækbar pumpe til den næste generation af bløde robotter
- Ikke en sikker platform:Indien forbyder Zoom til offentlig brug
- Skab åben datakultur for at fodre sulten verden, siger eksperter
- Forskere løser et halvt århundrede gammelt magnesiumdimer-mysterium
- Hvad er den omtrentlige temperatur på solen?


