Hvorfor rustes metal, og hvad er den kemiske reaktion til rustning?
Kemien i rust:
Rust eller jernoxid er en rødbrun forbindelse dannet, når jern reagerer med ilt i nærvær af vand eller fugt. Denne kemiske reaktion kaldes oxidation .
Her er sammenbruddet:
1. Jern (Fe) reagerer med ilt (O2) for at danne jernoxid (Fe2O3), også kendt som rust:
* 4Fe + 3O2 → 2Fe2O3
Denne reaktion er faktisk en kompleks proces, der involverer flere trin. Jernatomerne mister elektroner, og iltatomer får elektroner og danner positivt ladede jernioner (Fe3+) og negativt ladede oxidioner (O2-). Disse ioner kombineres derefter for at danne jernoxid.
2. Tilstedeværelsen af vand (H2O) fremskynder rustenprocessen:
* Vand fungerer som en elektrolyt, der giver ionerne mulighed for lettere at bevæge sig og lette den kemiske reaktion.
* Vand opløses også det beskyttende oxidlag, der dannes på jern, og udsætter metallet for yderligere oxidation.
3. Andre faktorer, der påvirker rustning:
* syrer: Sure miljøer kan fremskynde rusten, fordi de øger hastigheden for jernoxidation.
* salte: Salt i luften eller vandet kan også fremskynde rusten.
* Temperatur: Højere temperaturer øger generelt hastigheden af kemiske reaktioner, herunder rustning.
4. Resultatet:
Dannelsen af rust svækker jernet, hvilket gør det sprødt og tilbøjeligt til at bryde. Rust optager også mere plads end jern, hvilket får metallet til at udvide og potentielt revne.
Forebyggelse af rust:
* belægninger: Påføring af et beskyttende lag maling, olie eller andre belægninger forhindrer ilt og vand i at kontakte jernet.
* galvanisering: Belægning af jernet med et lag zink, som er mere modstandsdygtigt over for oxidation, beskytter jernet.
* legering: Tilføjelse af andre elementer, såsom krom, til jernet, kan gøre det mere modstandsdygtigt over for rustning.
At forstå rustens kemi hjælper os med at finde måder at forhindre det og bevare integriteten af jernstrukturer og genstande.
Sidste artikelHvilket element er ikke ædle gasser?
Næste artikelHvad er formelmassen af NIF2?
 Varme artikler
Varme artikler
-
 3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær
3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær -
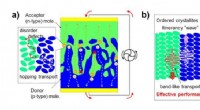 Sporing af ladningsbærere i den molekylære krystal ved organisk pn-forbindelse(a) Hoppeledning i uordnet kryds, (b) båndledning i krystallinsk forbindelse. Kredit:NINS/IMS I konventionelle organiske solceller, elektronerne udviser deres partikel-natur og skal hoppe mellem o
Sporing af ladningsbærere i den molekylære krystal ved organisk pn-forbindelse(a) Hoppeledning i uordnet kryds, (b) båndledning i krystallinsk forbindelse. Kredit:NINS/IMS I konventionelle organiske solceller, elektronerne udviser deres partikel-natur og skal hoppe mellem o -
 Undersøgelse viser potentiale for jordvenlig plasterstatningDen nye blanding af bioplast og gummi, der blev udtænkt af forskere i Ohio State, viste sig at være meget mere holdbar end bioplasten på egen hånd Credit:Ohio State University Stræben efter at hol
Undersøgelse viser potentiale for jordvenlig plasterstatningDen nye blanding af bioplast og gummi, der blev udtænkt af forskere i Ohio State, viste sig at være meget mere holdbar end bioplasten på egen hånd Credit:Ohio State University Stræben efter at hol -
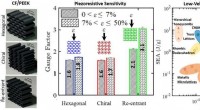 Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
- Sri Lanka forbyder motorsave, tømmerværker:formand
- Gemini South-teleskoper GHOST-spektrograf fanger de første lysobservationer af en lysstærk, kemisk…
- Kunne solen udvide og ødelægge alle planeter?
- Dødstallet stiger, efterhånden som tinder-tørre forhold tilfører dødbringende californiske bran…
- Udvikling af ikke-flygtige flydende anthracener til let luminescensjustering i fuld farve
- Forbindelse mellem kvinders våbenejerskab og øget politisk deltagelse


