Hvad er formelmassen af NIF2?
1. Find atommasserne i hvert element:
* ni (nikkel): 58.6934 g/mol
* f (fluor): 18.9984 g/mol
2. Multiplicer atommassen for hvert element med dets underskrift i formlen:
* ni: 1 x 58.6934 g/mol =58.6934 g/mol
* f: 2 x 18.9984 g/mol =37.9968 g/mol
3. Tilføj resultaterne sammen:
58.6934 g/mol + 37.9968 g/mol = 96.6902 g/mol
Derfor er formelmassen af NIF₂ 96.6902 g/mol.
Sidste artikelHvorfor rustes metal, og hvad er den kemiske reaktion til rustning?
Næste artikelRutherford afbildede atomet som en tæt?
 Varme artikler
Varme artikler
-
 Forskere introducerer nyt materiale til at opbevare brintKredit:Siberian Federal University Forskere fra Siberian Federal University og Institute of Physics af SB RAS producerede et nyt materiale til brintlagring. Materialet er baseret på magnesiumhydri
Forskere introducerer nyt materiale til at opbevare brintKredit:Siberian Federal University Forskere fra Siberian Federal University og Institute of Physics af SB RAS producerede et nyt materiale til brintlagring. Materialet er baseret på magnesiumhydri -
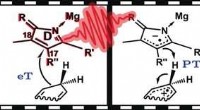 Trinvis hydridoverførsel i biosyntesen af klorofylHydridoverførsel er en vigtig reaktion for kemi (f.eks. brændstofceller), samt biologi (f.eks. respirationskæde og fotosyntese). Tit, en delreaktion involverer overførsel af en hydridion (H−). Men inv
Trinvis hydridoverførsel i biosyntesen af klorofylHydridoverførsel er en vigtig reaktion for kemi (f.eks. brændstofceller), samt biologi (f.eks. respirationskæde og fotosyntese). Tit, en delreaktion involverer overførsel af en hydridion (H−). Men inv -
 Syntese af et sjældent metalkompleks af dinitrogenoxid åbner nye udsigter forKredit:Monika Stolar og Chris Gendy Ligesom dets kemiske relative kuldioxid (CO 2 ), dinitrogenoxid (N 2 O) er en vigtig drivhusgas og det dominerende ozonnedbrydende stof, der udsendes i det
Syntese af et sjældent metalkompleks af dinitrogenoxid åbner nye udsigter forKredit:Monika Stolar og Chris Gendy Ligesom dets kemiske relative kuldioxid (CO 2 ), dinitrogenoxid (N 2 O) er en vigtig drivhusgas og det dominerende ozonnedbrydende stof, der udsendes i det -
 Dyrkning af HCA -krystallerKredit:ESS/Fisher Zoë Fisher og Katarina Koruza fra ESS Deuteration and Macromolecular Crystallization (DEMAX) Support lab og Lunds Universitet har brugt dampdiffusionsmetoder til at dyrke store p
Dyrkning af HCA -krystallerKredit:ESS/Fisher Zoë Fisher og Katarina Koruza fra ESS Deuteration and Macromolecular Crystallization (DEMAX) Support lab og Lunds Universitet har brugt dampdiffusionsmetoder til at dyrke store p
- Hvor mange typer månefaser kan ses af en observatør på jorden?
- Forskere bruger S-matrix bootstrap til at undersøge, om strengteori er den eneste konsistente teori…
- Webb-teleskop fanger farverige Cartwheel Galaxy
- Hvordan er jordens form og hvad indeholder?
- Sådan fungerer Earth 911.org
- Portugal sætter ny varmerekord i juli og forværrer alvorlig tørke


