Hvad blev bevist forkert ved strukturen af Niels Bohr Atom?
1. Elektron orbitaler:
* Bohrs model: Foreslog, at elektroner kredser om kernen i faste, cirkulære stier kaldet kredsløb, svarende til planeter, der kredser om solen.
* virkelighed: Kvantemekanik viste, at elektroner ikke kredserer i faste stier. I stedet besætter de orbitaler , som er tredimensionelle rumområder, hvor sandsynligheden for at finde en elektron er høj. Disse orbitaler er ikke enkle cirkulære stier, men snarere komplekse former.
2. Elektronenerginiveau:
* Bohrs model: Forklarede, at elektroner kun kunne eksistere i specifikke energiniveauer og ville hoppe mellem dem ved at absorbere eller udsende fotoner.
* virkelighed: Mens begrebet kvantiseret energiniveau var korrekt, forenklede modellen virkeligheden. Kvantemekanik viste, at elektroner ikke hopper øjeblikkeligt mellem niveauer, men snarere gennemgår overgange der kan involvere mellemenergitilstande.
3. Spektrale linjer:
* Bohrs model: Forklarede med succes emissionsspektret af brint og forudsagde de observerede linjer.
* virkelighed: Det kunne ikke præcist forudsige de spektrale linjer af atomer med flere elektroner. Kvantemekanik gav en mere komplet forklaring på kompleksiteten af spektrale linjer.
4. Elektronspin:
* Bohrs model: Tagede ikke for den iboende vinkelmoment for elektroner, kendt som spin.
* virkelighed: Elektronspin er en grundlæggende egenskab ved elektroner og spiller en afgørende rolle i atomstruktur og kemisk binding.
5. Atomstruktur:
* Bohrs model: Foreslog en enkel, planetarisk struktur med elektroner, der kredser om kernen.
* virkelighed: Kvantemekanik viste, at kernen er omgivet af en sky af elektroner, der besætter orbitaler, ikke faste kredsløb. Dette førte til udviklingen af mere sofistikerede modeller af atomstruktur.
generelt:
Mens Niels Bohrs model var en betydelig fremgang, var det et forenklet billede af atomet. Kvantemekanik gav en meget mere nøjagtig og kompleks forståelse af elektronernes opførsel og atomernes struktur. Bohrs model er dog stadig et værdifuldt værktøj til at forstå grundlæggende begreber om atomstruktur.
Sidste artikelHvad er der inde i et atom?
Næste artikelHvad er det kemiske navn på MGC2O4?
 Varme artikler
Varme artikler
-
 Team udvikler meget strækbare hydrogeler til 3D-udskrivning i multimateriale i høj opløsningMeget strækbare og UV -hærdende 3D -print -hydrogeler, der kan strækkes med op til 1300% og er kompatible med højopløselig digital lysbehandlingsbaseret 3D -udskrivning, der muliggør fremstilling af h
Team udvikler meget strækbare hydrogeler til 3D-udskrivning i multimateriale i høj opløsningMeget strækbare og UV -hærdende 3D -print -hydrogeler, der kan strækkes med op til 1300% og er kompatible med højopløselig digital lysbehandlingsbaseret 3D -udskrivning, der muliggør fremstilling af h -
 Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering
Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering -
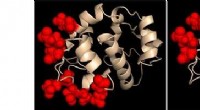 Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst
Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst -
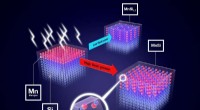 Særlig varmebehandling forbedrer nyt magnetisk materialeHvis forskerne varierer blinkens magt, de kan præcist påvirke forholdet mellem de forskellige krystalfaser. Kredit:HZDR/Juniks Skyrmions - små magnetiske hvirvler - betragtes som lovende kandidate
Særlig varmebehandling forbedrer nyt magnetisk materialeHvis forskerne varierer blinkens magt, de kan præcist påvirke forholdet mellem de forskellige krystalfaser. Kredit:HZDR/Juniks Skyrmions - små magnetiske hvirvler - betragtes som lovende kandidate
- Hvordan hjælper et kalejdoskop os?
- Sådan beregnes væksthastighed eller procentvis ændring
- Hvad er Western Blot Test?
- Hvordan kolibrier udviklede sig til at flyve i stor højde
- Tilfældig kinetisk energi, der er besat af genstande i et materiale ved endelig temperatur, et obje…
- Hvilken organelle fremstiller hver af de 4 makromolekyler?


