Hvad overvejes et vandmolekyle, når ilt trækker elektroner tættere?
* kovalent binding: Oxygen- og brintatomerne deler elektroner til dannelse af bindingen.
* polær: Oxygen er mere elektronegativ end brint, hvilket betyder, at det har en stærkere tiltrækning til elektroner. Dette får de delte elektroner til at tilbringe mere tid tættere på iltatomet, hvilket giver det en let negativ ladning (Δ-) og brintatomerne en let positiv ladning (Δ+).
Denne ujævne fordeling af ladning inden for molekylet gør det polar , hvilket betyder, at det har en positiv og en negativ ende. Denne polaritet er afgørende for mange af vandets unikke egenskaber, såsom dens evne til at opløse mange stoffer og danne brintbindinger.
Sidste artikelHvordan er kviksølv og natrium forskellige?
Næste artikelHvor mange molekyler i ammoniumchlorid?
 Varme artikler
Varme artikler
-
 Svovlfjernende bakterier kan være nøglen til at lave fælles komponent i plastikForskere har opdaget, hvordan mikrober i vandlidende jorde producerer høje niveauer af ethylen, hvilket kan have en negativ indvirkning på landbrugsafgrøder og bioenergiråvarer som skiftegræs. Denne n
Svovlfjernende bakterier kan være nøglen til at lave fælles komponent i plastikForskere har opdaget, hvordan mikrober i vandlidende jorde producerer høje niveauer af ethylen, hvilket kan have en negativ indvirkning på landbrugsafgrøder og bioenergiråvarer som skiftegræs. Denne n -
 Forskere opdager ny elektrokatalysator til at omdanne kuldioxid til flydende brændstofKunstnerisk gengivelse af elektrokatalytisk proces til omdannelse af kuldioxid og vand til ethanol. Kredit:Kredit:Argonne National Laboratory Katalysatorer fremskynder kemiske reaktioner og danner
Forskere opdager ny elektrokatalysator til at omdanne kuldioxid til flydende brændstofKunstnerisk gengivelse af elektrokatalytisk proces til omdannelse af kuldioxid og vand til ethanol. Kredit:Kredit:Argonne National Laboratory Katalysatorer fremskynder kemiske reaktioner og danner -
 Ny test identificerer hurtigt antibiotikaresistente superbugsTara deBoer rummer en brøndtallerken med syntetiske urinprøver, der er føjet til DETECT-opløsningen. Opløsningen bliver gul, når der er antibiotikaresistente bakterier til stede. Kredit:Stephen McNall
Ny test identificerer hurtigt antibiotikaresistente superbugsTara deBoer rummer en brøndtallerken med syntetiske urinprøver, der er føjet til DETECT-opløsningen. Opløsningen bliver gul, når der er antibiotikaresistente bakterier til stede. Kredit:Stephen McNall -
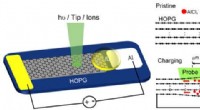 Overfladeeffekt af elektroder afsløret ved operando overfladevidenskabelige metoderSkematisk af Al/HOPG planar batteri. Kredit:@Science China Press Overflade og grænseflade spiller en afgørende rolle i energilagringsenheder, kræver derfor in-situ/operando-metoder til at sonde de
Overfladeeffekt af elektroder afsløret ved operando overfladevidenskabelige metoderSkematisk af Al/HOPG planar batteri. Kredit:@Science China Press Overflade og grænseflade spiller en afgørende rolle i energilagringsenheder, kræver derfor in-situ/operando-metoder til at sonde de
- Forskning viser løfte om ny enhed til at opdage sygdom med dråbe blod
- Overkropsstyrke nøglefaktor for mænds kropslige attraktivitet
- Olie og vand kan blandes under ekstremt tryk
- Brugerkontrol og gennemsigtighed er nøglen til tillid til personlige mobilapps
- Ledetråde om, hvordan jord kan reagere på fundet af klimaændringer
- Hvordan våben giver næring til Amerikas masseskyderier


