Ioniske bindinger dannes, hvornår?
et atom mister en elektron (bliver positivt ladet) og et andet atom vinder, at elektron (bliver negativt ladet).
Dette skaber en stærk elektrostatisk attraktion mellem de to modsat ladede ioner og holder dem sammen.
Her er en sammenbrud:
* metaller har en tendens til at miste elektroner, danne kationer (positivt ladede ioner).
* ikke -metaller har en tendens til at vinde elektroner, danne anioner (negativt ladede ioner).
Nøgleegenskaber ved ionisk binding:
* høje smelte- og kogepunkter: Den stærke elektrostatiske attraktion mellem ioner kræver en masse energi til at bryde.
* fast ved stuetemperatur: De stærke kræfter holder ionerne i en stiv, krystallinsk struktur.
* gode ledere af elektricitet, når de er opløst eller smeltet: Den frie bevægelse af ioner muliggør strøm af elektrisk strøm.
* sprød: Den stive struktur gør dem modtagelige for at bryde, når de er stressede.
Eksempler:
* NaCl (bordsalt): Natrium (NA) mister et elektron for at blive Na+, og chlor (CL) vinder, at elektronet bliver Cl-. De resulterende ioner tiltrækkes af hinanden og danner en ionisk binding.
* mgo (magnesiumoxid): Magnesium (Mg) mister to elektroner for at blive Mg2+, og ilt (O) får disse to elektroner til at blive O2-.
 Varme artikler
Varme artikler
-
 Forbedring af kvantecomputereKredit:CC0 Public Domain I årtier, eksperter har forudsagt, at kvantecomputere en dag vil udføre vanskelige opgaver, såsom simulering af komplekse kemiske systemer, det kan ikke lade sig gøre med
Forbedring af kvantecomputereKredit:CC0 Public Domain I årtier, eksperter har forudsagt, at kvantecomputere en dag vil udføre vanskelige opgaver, såsom simulering af komplekse kemiske systemer, det kan ikke lade sig gøre med -
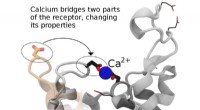 Forstå en celles dørklokkeFremme af design af lægemidler til bedre medicinske effekter kræver en kombination af eksperimentel og computersimuleringsforskning. Forskere ved Los Alamos National Laboratory, University of Toronto,
Forstå en celles dørklokkeFremme af design af lægemidler til bedre medicinske effekter kræver en kombination af eksperimentel og computersimuleringsforskning. Forskere ved Los Alamos National Laboratory, University of Toronto, -
 Kender du vejen til Berkelium, Californium?Forskere ved Berkeley Labs forgænger, UC Radiation Laboratory, opdagede berkelium i 1949, og californium i 1950. I dag, Berkeley Lab-forskere bruger avancerede instrumenter på Molecular Foundry for be
Kender du vejen til Berkelium, Californium?Forskere ved Berkeley Labs forgænger, UC Radiation Laboratory, opdagede berkelium i 1949, og californium i 1950. I dag, Berkeley Lab-forskere bruger avancerede instrumenter på Molecular Foundry for be -
 Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud
Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud
- Hvordan ser planeten Mars ud fra rummet?
- Hvem var den første videnskabsmand, og hvad han opfandt?
- Hvordan et kæmpe nedslag dannede asteroiden Vestas 'bælte'
- Hvad er den type binding, zink og vil have?
- Landbrugsbrande i Brasilien skader spædbørns sundhed, en advarsel til udviklingslandene
- Forskere fremmer forståelsen af vitale enzymer


