Forstå en celles dørklokke
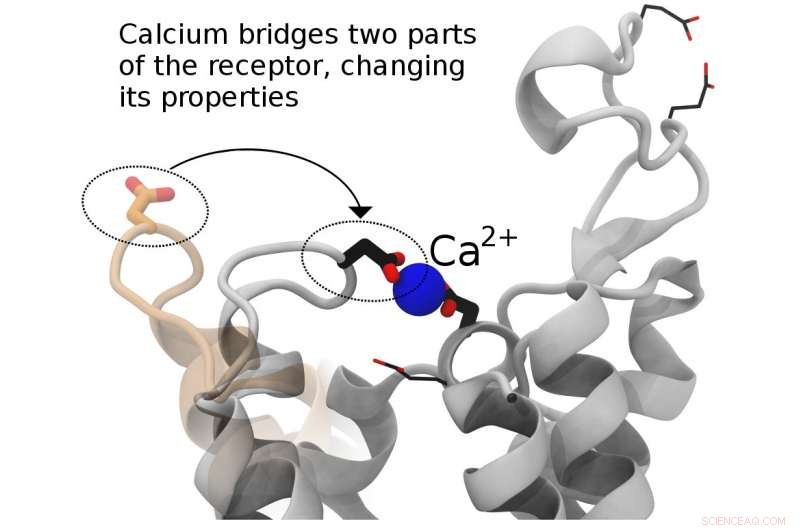
Fremme af design af lægemidler til bedre medicinske effekter kræver en kombination af eksperimentel og computersimuleringsforskning. Forskere ved Los Alamos National Laboratory, University of Toronto, Canada, University of California, San Diego og Kwansei Gakuin University, Japan er ved at udforske, hvordan cellulære komponenter kommunikerer med forskellige nærliggende molekyler. På dette billede, calcium danner bro mellem to dele af en cellereceptor, muligvis regulere dens aktivitet. Kredit:Los Alamos National Laboratory
Et multi-institutionelt projekt for at forstå et af hovedmålene for design af humant lægemiddel har frembragt ny indsigt i, hvordan strukturel kommunikation fungerer i en cellekomponent kaldet en G-proteinkoblet receptor (GPCR'er), dybest set en "dørklokke" struktur, der advarer cellen om vigtige molekyler i nærheden. En dybere forståelse af receptorens struktur og funktion vil muliggøre bedre lægemiddeludvikling.
"Det er et stort felt af aktiv forskning i den akademiske verden og industrien, for hvis vi kan finde ud af præcis, hvordan GPCR'er fungerer, så kan vi lettere designe stoffer til at ændre deres adfærd og derved kontrollere smerte, sult, og mere, " sagde medforfatter Christopher Neale, en forsker ved Center for Ikke-lineære Studier ved Los Alamos National Laboratory. "Dette arbejde hjælper os med at forstå receptorernes funktion som et middel til at muliggøre fremtidig opdagelse af lægemidler. F.eks. hvis calciumbinding kan slå en GPCR fra, så kan man bruge den viden i en guidet søgen efter lægemidler, der enten fremmer eller hæmmer calciumbinding afhængigt af det ønskede sundhedsresultat."
GPCR'er er en familie af membranproteiner, der overfører information til vores celler. De reagerer på ting som adrenalin og opioider, og de er den største klasse af humane lægemiddelmål. Undersøgelsen rapporterede i denne uge i Naturkommunikation beskriver reguleringen af GPCR'er af fysiologiske ioner såsom natrium, calcium og magnesium.
Papiret skitserer in vitro kernemagnetiske resonanseksperimenter udført af Scott Prossers gruppe (University of Toronto, Canada), der identificerede ændringer i disse receptorer baseret på divalente kationkoncentrationer. Papiret inkluderer bekræftelse af disse virkninger i levende celler af Roger Sunaharas gruppe (University of California, San Diego) og computersimuleringer kørt i Los Alamos af Neale og Angel E. Garcia for at definere atomopløsningsmekanismer, der kan forklare de eksperimentelle resultater. Endelig, yderligere teori af Adnan Sljoka (Kwansei Gakuin University, Japan) viste, at de mekanismer, som Neale foreslog, involverer mulige typer af strukturel kommunikation gennem receptoren.
 Varme artikler
Varme artikler
-
 Hvordan vi fandt den tidligste glasproduktion syd for Sahara, og hvad det betyderGlasrelaterede artefakter udgravet fra Igbo Olokun, Ile Ife. Til venstre:glasperler, Til højre:fragmenter af glas fremstiller digler. Kredit:Abidemi Babatunde Babalola Menneskehedens historie fra
Hvordan vi fandt den tidligste glasproduktion syd for Sahara, og hvad det betyderGlasrelaterede artefakter udgravet fra Igbo Olokun, Ile Ife. Til venstre:glasperler, Til højre:fragmenter af glas fremstiller digler. Kredit:Abidemi Babatunde Babalola Menneskehedens historie fra -
 Hvorfor er bomuldsabsorberende?De mest effektive badehåndklæder er lavet af 100 procent bomuld, fordi bomuld er mest effektiv til at absorbere eller opsuge vand. Bomuld er i stand til at absorbere op til 27 gange sin vægt i flydend
Hvorfor er bomuldsabsorberende?De mest effektive badehåndklæder er lavet af 100 procent bomuld, fordi bomuld er mest effektiv til at absorbere eller opsuge vand. Bomuld er i stand til at absorbere op til 27 gange sin vægt i flydend -
 Registrering af spormængder af flere klasser af antibiotika i fødevarerKredit:American Chemical Society Udbredt brug af antibiotika i menneskers sundhedspleje og husdyrhold har ført til, at spormængder af stofferne ender i fødevarer. Langtidsforbrug kan forårsage sun
Registrering af spormængder af flere klasser af antibiotika i fødevarerKredit:American Chemical Society Udbredt brug af antibiotika i menneskers sundhedspleje og husdyrhold har ført til, at spormængder af stofferne ender i fødevarer. Langtidsforbrug kan forårsage sun -
 Kunstigt enzym kan aktivere et genskifteLad der være lys:Et kunstigt metalloenzym (blåt) trænger ind i en pattedyrscelle, hvor det fremskynder frigivelsen af et hormon (blå til røde kugler). Dette aktiverer en genkontakt (cirkler med pile
Kunstigt enzym kan aktivere et genskifteLad der være lys:Et kunstigt metalloenzym (blåt) trænger ind i en pattedyrscelle, hvor det fremskynder frigivelsen af et hormon (blå til røde kugler). Dette aktiverer en genkontakt (cirkler med pile
- Hæmning af HER2 på tumorceller af molekylært prægede nanopartikler
- Ny nanoteknisk strategi viser potentiale for forbedret avanceret energilagring
- Med mere raffinerede ganer, Kina tørster efter vin vokser
- Video:Sådan virker dobbeltvirkende bagepulver to gange
- Flyvende blind:Apps hjælper synshandicappede med at navigere i lufthavnen
- En ny solcreme, der ikke trænger ind i huden


