Hvad er processen, når en solid vender sig til gas?
1. Energiabsorption:
* Faste partikler har et fast arrangement og holdes sammen af stærke intermolekylære kræfter.
* Når nok varmeenergi absorberes af det faste stof, får partiklerne kinetisk energi og begynder at vibrere hurtigere.
2. Overvinde intermolekylære kræfter:
* Når den kinetiske energi øges, bliver vibrationerne så stærke, at de overvinder de intermolekylære kræfter, der holder partiklerne sammen.
* Partiklerne slipper fri fra deres faste struktur.
3. Overgang til gas:
* De frigjorte partikler bevæger sig nu tilfældigt og uafhængigt og fylder den tilgængelige plads.
* Dette er den gasformige tilstand, hvor partiklerne er langt fra hinanden og har svage intermolekylære kræfter.
Eksempler på sublimering:
* Tøris (fast kuldioxid) sublimerer til kuldioxidgas. Dette er et almindeligt eksempel, da tøris ikke smelter i en flydende tilstand.
* naphthalen (mothballs) forsvinder over tid. Den faste naphthalen sublimeres langsomt i luften.
* frosset vand (is), der drejer til vanddamp (gas) i koldt, tørt klima. Sådan forsvinder frost på kolde overflader.
Faktorer, der påvirker sublimering:
* Temperatur: Højere temperaturer giver mere energi for partiklerne til at overvinde intermolekylære kræfter.
* tryk: Lavere tryk gør det muligt for partiklerne lettere at undslippe i den gasformige tilstand.
* Stof: Forskellige stoffer har forskellige styrker af intermolekylære kræfter, der påvirker deres lethed af sublimering.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Venstre eller højre? Ny algoritme tager chiralitetsbestemmelse til næste niveauKredit:HIMS / RSC Forskere ved Molecular Photonics-gruppen under Van t Hoff Instituttet for Molekylær Videnskab ved Universitetet i Amsterdam har væsentligt forbedret den eksperimentelle bestemmel
Venstre eller højre? Ny algoritme tager chiralitetsbestemmelse til næste niveauKredit:HIMS / RSC Forskere ved Molecular Photonics-gruppen under Van t Hoff Instituttet for Molekylær Videnskab ved Universitetet i Amsterdam har væsentligt forbedret den eksperimentelle bestemmel -
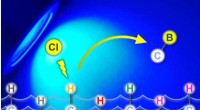 Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner
Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner -
 Ultrahurtig kompression tilbyder en ny måde at få makromolekyler ind i cellerneBilledet viser en mikrofluidisk chip, hvortil der er tilføjet farvestof for at vise kanalerne. Ved at behandle levende celler som små svampe, forskere har udviklet en potentielt ny måde at introducere
Ultrahurtig kompression tilbyder en ny måde at få makromolekyler ind i cellerneBilledet viser en mikrofluidisk chip, hvortil der er tilføjet farvestof for at vise kanalerne. Ved at behandle levende celler som små svampe, forskere har udviklet en potentielt ny måde at introducere -
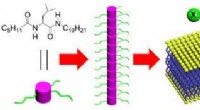 En ny metode til at transportere ioner gennem cellemembraner baseret på en enkelt aminosyreEkstremt simple monopeptider samler sig selv til stavlignende strukturer og videre til ringformede ensembler til mediering af højeffektiv transport af anioner i membranen. Kredit:Agency for Science, T
En ny metode til at transportere ioner gennem cellemembraner baseret på en enkelt aminosyreEkstremt simple monopeptider samler sig selv til stavlignende strukturer og videre til ringformede ensembler til mediering af højeffektiv transport af anioner i membranen. Kredit:Agency for Science, T
- Saturn-tågens mærkelige strukturer
- Erhvervsskoleforskningen er gået i stykker - her kan du løse det
- Galileo var den første person til at se måner af Uranus eller Jupiter?
- Hvorfor er vand et godt valg at varme noget?
- Hvordan påvirker temperaturinversioner luftforurening?
- Hvad er den faktiske dato uden springår og besparelser i dagslys?


